von Joachim Lorenz, Karlstein a. Main
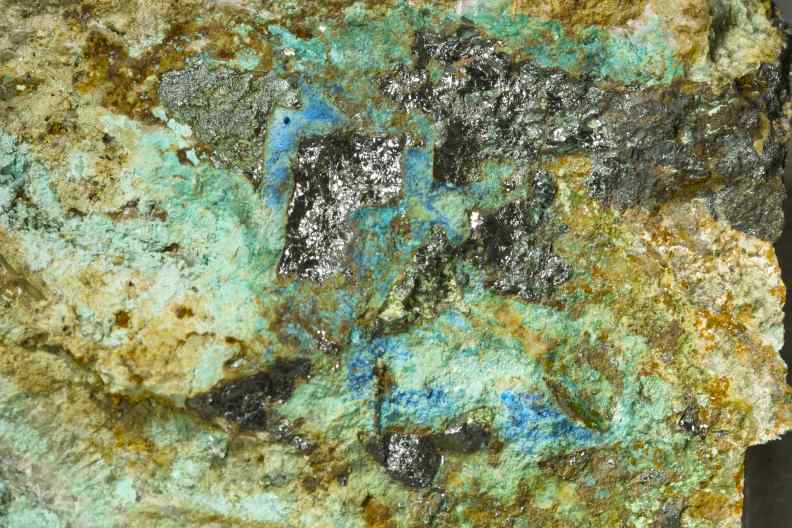
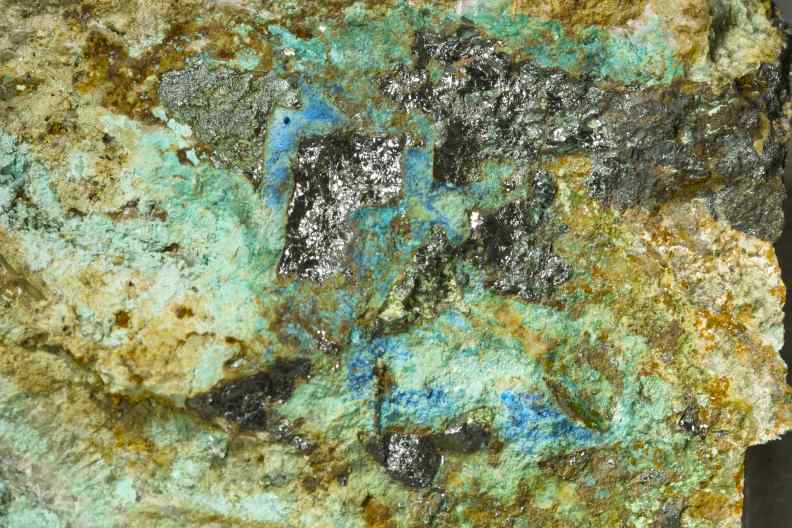




 Ist
das wirklich gefährlich?
Ist
das wirklich gefährlich? 
Die geogen bedingt und für den Durchschnitt in Deutschland hohen As-Gehalte des Spessarts (und anderer Regionen) lassen regelmäßig die Adern von Bauherren und Baufirmen anschwellen. Der Grund ist der Umstand, dass aller Fels und Erde nach dem Bewegen als "Abfall" deklariert werden muss. Wenn man den dann an Ort und Stelle doch nicht verwerten kann, muss der Aushub usw. von Baustellen "entsorgt" werden. Dann werden chmische Analysen erstellt und mit den Abfall gelten Zuordungswerte aus der LAGA-Liste (Anonym 2003) verglichen. Dieses Werk sollte eigentlich für anthropogene Abfälle gelten, schließt aber aber merkwürdigerweise die natürlichen Steine und Erden ein. In diesem Werk werden Zuordnungwerte definiert, die für Abfall nicht überschritten werden dürfen; für Arsen sind dies:
Z O 20 g/t
Z 1.1 30 g/t
Z 1.2 50 g/t
Z 2 150 g/t.
Diese Einstufung wird ohne Rücksicht auf die Bindung, auf die pH-Wert des Bodens und der Umgebung vorgenommen. Und man geht beim Vorschriftensetzer einfach davon aus, dass der Grund und Boden immer "unbelastet" ist, also die Werte von ZO unterschreitet; das mag in weiten Teilen Norddeutschlands mit den ausgelaugten und letztendlich aus Skandinavien stammenden Kies- und Sandflächen auch so sein.
In den Mittelgebirgen sieht das völlig anders aus; man denke beispielsweise an die Bergbauregionen in Schwarzwald, Harz und Erzgebirge. Da ein Einbau von "belasteter" Erde und Felsen in eine Reihe von Flächen nicht zulässig ist (Trinkwasserschutzgebiete, Spielplätze, Naturschutzgebiete usw., müssen große Massen umgelagert werden. Dies führt im (Vor-)Spessart dazu, dass große Volumen an Erdreich zu Sonderdabfall erklärt werden, die dann sehr kostenintensiv entsorgt werden müssen oder durch halb Deutschland gefahren werden (das kostet auch Geld). Damit wird niemanden geholfen, denn das nicht bewegete Material in der Umgebung ist ja genauso reich an Spurenstoffen. Da es sich um weiträumige Anomalien handelt und die Baumaßnahmen nur punktuell sind, ändert sich in der Fläche kaum etwas. In Unkenntnis der wahren Verhältnisse schafft man mit den Erdaushubdeponien (die nur ZO/Z1 einbauen dürfen, aber in einem Bereich liegen, der als Z2 eingestuft werden müsste) Bereiche schafft, die weniger Spurenstoffe enthalten wie die Umgebung! Würde man diese Werte der LAGA-Liste in der Fläche anwenden wollen, müsste man weite Teil des Spessarts sanieren, was völlig sinnlos ist - und auch unbezahlbar wäre. Dies würde besonders die Flächen betreffen, auf denen der Kupferschiefer ausstreicht und die Zonen, die von Schwerspatgängen bzw. gangförmigen Mineralisationen durchzogen sind.
Hier wäre der Gesetzgeber und Vorschriftenersteller - wie die LAGA - gefordert, diesen länderübergreifenden Blödsinn abzuschaffen. Einmal müsste man trennen zwischen anthropogenen und geogenen Spurenstoffen, denn die geogenen Werte sind gegeben und nicht änderbar. Ob man jede anthropene Anomalie beseitigen muss, ist sehr fraglich, insbesondere wenn die aus römischer Zeit oder aus dem Mittelalter stammt. Nach den chemischen Analysen wäre es den geologisch-chemisch versierten Gutachtern nach der Auswertung der Proben zu überlassen, anschließend darzulegen, dass trotz der "hohen" Schwermetall-Werte keine Besorgnis für eine Verwertung bzw. dem Einbau zu erwarten wäre. Dabei wären die Randparameter wie Gesteinschemie, pH-Werte und Löslichlichkeit zu berücksichtigen (z. B. auch beim Zink, der im chemisch sehr beständigen Staurolith eingebaut sein kann).
Übrigens wächst auf den "hoch belasteten" Flächen des Spessarts einen ganz normale Vegetation. Und für die typischen Schwermetallzeiger (z. B. das "Galmei-Veilchen") sind die Gehalte wohl noch zu klein. Oder wurde die Pflanze nicht hierher verschleppt.
Was im Spessart das Arsen ist, wird im nahen Vogelsberg durch die in der Fläche verbreiteten vulkanischen Gesteine erzeugt: dort sind es die Gehalte an Chrom und Nickel (sie stammen aus dem Oberen Erdmantel), die ebenfalls die Werte der LAGA-Liste überschreiten.


Unscheinbarer, brauner Tilasit (ein wasserfreies Arsenat
mit der idealen Formel CaMg[F/AsO4] und einem Gehalt
von ca. 51 Gew.-% Arsenoxid) als frei gewachsene Kristalle in
einer Kluft zusammen mit Carbonaten (darunter leicht rosafarbener
Rhodochrosit) auf dem Rhyolith von Sailauf,
Bilbreite jeweils 5 mm (die Kristalle im rechten Foto wurden mit
verdünnter Salzsäure frei gelegt*), gefunden 1994. Das Mineral
kommt weltweit nur an ganz wenigen Orten vor. Dies hat seinen
Grund darin, dass es nur ganz selten die zur Bildung notwendigen
chemisch-pyhikalischen Bedingungen gab, unter denen diese
Kristalle gebildet werden konnten. Aber Tilasit ist isotyp mit
Titanit (CaTi[O/SiO4]), d. h. es hat den gleichen
Strukturtyp, so dass statt des SiO4-Tertaeders eine AsO4-Gruppe
eingebaut werden kann, was zu merklichen As-Gehalten führen
kann.
*Dies bedeutet, dass die Verbindung so stabil ist, dass verdünnte
Salzsäure dem nichts anhaben kann. Würde man so was essen - was freiwillig niemand tun würde
-, dann könnte das Arsen auch im sauren Magen nicht gelöst werden
und man würde die Kristalle auch wieder so ausscheiden, ohne
nennenswerten Mengen an Arsen aufzunehmen.

Silbriger Nickel-Skutterudit ((Co,Ni)AsS, mit 63 - 71 %
Gew.-% As) in der Form von kuboktaedrischen Kristallen im
hellbraunem Siderit aus Bieber, gefunden
sicher vor 1867, Bildbreite 3 cm. Das Kobalterz ist auch gegenüber
einem kurzzeitigen Einwirken von Säure stabil, aber verwittert an
der Erdoberfläche schnell. Das As wird aber durch die Bestandteile
der Gangart aus Siderit kurzfristig gebunden*. Die Bergbauhalden
des 18. und 19. Jahrhunderts geben erhebliche As-Konzentrationen
frei, die von den Niederschlägen abhängen: wenig Regen bringt hohe
As-Gehalte, viel Niederschlag erzeugt geringe Gehalte infolge
einer Verdünnung bzw. der geringeren Verweildauer des Wassers im
Haldenkörper und damit einem geringeren Lösungsvermögen.
*Werden solche Stücke in feuchten Sammlungen über Jahrzehnte
aufbewahrt, so bildet sich eine farblose Kruste aus Arsenolith
aus. Es ist die natürliche Form des Arseniks und besteht aus
winzigen farblosen Oktaedern.
Als man in Schwarzenfels (heute Mottgers) im 18. und 19.
Jahrhundert die hoch arsenhaltigen Kobalterze aus Bieber zu der
blauen Smalte verarbeitete, wurde das Arsen abgetrennt und dann
als Fliegengift oder Zusatz für die Glasherstellung verkauft. Die
Produktion belief sich auf einige Tonnen im Jahr!
Aus Analysen von Gläsern der Glashütte Emmerichsthal (im
Steinbachtal, südwestlich von Jossa gelegen, Markt Obersinn ) ist
bekannt, dass hier Arsenoxid statt Manganoxid als Oxidationsmittel
zur Beseitigung der durch das Eisen erzeugten, unerwünscht grünen
Farbe zugesetzt wurde (FITZ 1984:142). Die abgelegen liegende
Glashütte war von 1768 bis 1826 im Betrieb - seit 1814 zu Bayern
gehörend.
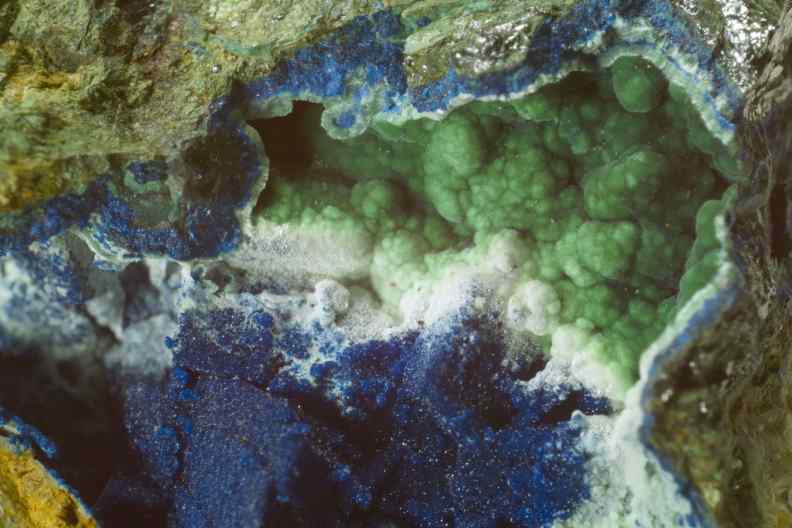
Weißer bis grüner, radialfaseriger Olivenit (Cu2[OH/AsO4],
mit ca. 40 % Gew.-% Arsenoxid) zusammen mit blauem Azurit und
silbrigem Tennantit (rechts oben) aus dem ehemaligen und für
Azurit so berühmten Steinbruch in Altenmittlau,
Bildbreite 12 mm, gefunden um 1990. Das Beispiel zeigt, was mit
dem aus dem Tennantit frei werdenden As passiert. Infolge der
bereit stehenden Kupfer-Ionen bei einem hohen Ca/Mg-Spiegel in dem
Hohlrum wird das As mit dem Cu gleich nebenan wieder als Olivenit
fixiert. Erst bei einer Lagerung an der Oberfläche würde diese
wenig stabile Verbindung durch die Kohlensäure gelöst und das As
würde neuerlich frei werden. Auch hier würde das reaktionsfreudige
Arsenat wieder einen Komplex mit den allgenwärtigen Eisen eingehen
und beispielsweise Skorodit bilden, den man von anthropogenen
Bergwerkshalden kennt.

Auch der gelbe Mimetestit - hier auf Ankerit - enthält
Arsen (Pb5[AsO4]3Cl, mit 23 Gew-%
Arsenoxid). Das Stück stammt aus Altenmittlau, wurde 1977 gefunden
und der Ausschnitt ist 2 cm breit. Das auffallende Mineral mit der
Apatit-Struktur kann Mischkristalle mit dem Phosphat Pyromorphit
bilden, in dem das AsO4-Ion (Arsenat) durch das PO4-Ion
(Posphat) ausgetauscht wird. Dies verhält sich chemisch sehr
ähnlich. Dies ist auch der Grund, warum Phosphat-haltige
Düngemittel - je nach Herkunft und Aufbereitung - oft etwas Arsen
enthalten (2 - 1.200 g/t). In Altenmittlau stammen die
Schwermetalle aus dem hier noch unterliegenden Kupferschiefer.
Infolge der Randlage am Spessart wurden die Metalle
tiefhydrothermal im Rahmen der Barytgenese mobilisiert und in den
bunten Mineralien der Klüfte und Drusen wieder ausgeschieden.
Neben dem Arsen wurden auch die Metalle Blei, Kupfer, Molybdän,
Barium, Zink, Mangan und Eisen transportiert. In den Randgebieten
des Zechsteinmeers wurde kein Kupferschiefer abgelagert, so dass
hier die große Menge an Schwermetallen fehlen. Aus diesem Grund
gibt es beispielsweise in Kleinostheim, Feldkahl, Schweinheim oder
Soden keine bunten Mineralien im Zechstein-Dolomit.
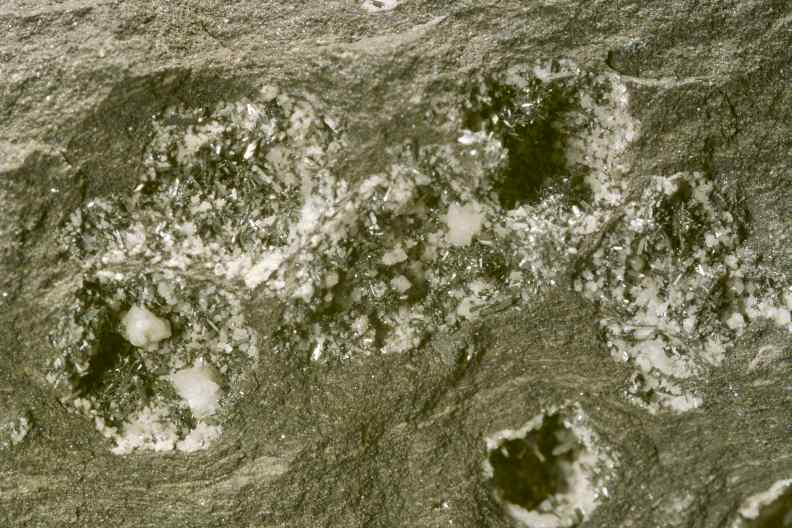
Silbrig glänzende, nadelige Arsenopyrit-Kristalle
(FeAsS mit ca. 49 % Arsen) zusammen mit weißem Dolomit im
schwarzen Kupferschiefer aus dem Raum Bieber, gefunden sicher im
19. Jahrhundert. Das Erz wurde von den alten Bergleuten als der
"Mißpickel" bezeichnte, weil man aus dem schweren Erz keine
Wertmetalle erzeugen konnte - außer Arsen, deshalb auch der Name
Arsenkies oder auch "Giftkies". Es ist eine sehr stabile
Verbindung, so dass das darin enthaltene Arsen im biologischen
Umfeld kurzfristig nicht frei wird. Aber infolge der weiten
Verbreitung als nicht mit dem bloßen Auge sichtbarer Bestandteil
im Kupferschiefer trägt das Mineral in einem erheblichen Teil zum
Arsengehalt im Kupferschiefer bei. Bemerkenswert ist weiter, dass
es beim Arsenopyrit eine deutliche Affinität zu Zinn- und
Goldlagerstätten gibt, d. h. Arsenopyrit kommt häufig in solchen
Lagerstätten vor, z. in der Goldlagerstätte von Brandholz bei
Goldkronach im Fichtelgebirge.
Arsenopyrit ist weltweit die größte Quelle für die Gewinnung von
Arsen; 2010 wurden 54.500 t Arsen produziert. Aus diesem wird dann
z. B. Calciumarsenat erzeugt, welches als
Schädlingsbekäpfungsmittel Verwendung findet. Auch zur
Konservierung von Holz finden Arsenverbindungen Anwendung. Die
früher verbreiteten Arsenfarben "Schweinfurter Grün" (Cu(CH3COO)2·3Cu(AsO2)2)
und "Scheeles Grün" (CuHAsO3) werden nicht mehr
großtechnisch hergestellt. Mit ihnen wurden früher Stoffe,
besonders Tapeten, aber auch Bücher und Wandfarben schön grün
gefärbt. Damit stürzte man ein ganzes Land ins Unglück (HAWKSLEY
2018).

Nahezu schwarzer Lithiophorit (mit der idealisierten chem.
Formel Al2LiMn4+2Mn3+O6(OH)6)
als Kluftbelag im Quarzit von Hemsbach in dem großen Steinbruch am Hahnenkamm, Bildbreite 5 cm,
gefunden 1997. Das Mineral dürfte nach der Formel gar kein Arsen
enthalten. Und es weit entfernt von den klassischen
Mineralisationen des Spessarts gebildet worden. Aber da auch hier
As-Ionen bei der Kristallisation vorhanden waren, wurde auch hier
As eingebaut bzw. als Besonderheit in der sehr komplexen Struktur
adsorbiert, so dass bei einer Analyse auch deutlich As
nachgeweisen werden kann; bei den Eisenoxiden ist das auch so,
deshalb werden poröse Eisenoxide wie Aktivkohle verwandt, um aus
dem Trinkwasser das As zu entfernen (LORENZ 2010:802f). Wurde
früher aus dem harten Gestein Schotter produziert, so gelangten
die Mangan- und Eisenerze in den Schotter und bei einer
Mischanalyse konnte man dann auch darin Arsen nachweisen. Aber
auch hier ist es unter natürlichen Bedingungen nicht mobil, so
dass es weiter an die Mangan- und Eisenoxide fixiert ist und so
den Pflanzen nicht zur Verfügung steht.

Typischer Haldenfund aus den Bergbaugebiet von Bieber:
Rosafarbener, erdiger und nur sehr lose aufliegender Erythrin
(Co3[AsO4]2·8H2O mit
etwa 38 % Arsenoxid und oft noch deutlichen Gehalten an Nickel)
auf einem Stück Calcit mit Hämatit (nicht sichtbar; Bildbreite 10
cm, gefunden 1985). Die im Haldenkörper vagabundierenden As-Ionen
aus den Sulfiden und Arseniden wurden hier durch die Ca-Ionen des
Gangstückes gefällt und es entstand die "Kobaltblüte". Durch die
Farbe fällt es sofort auf und aus diesem Grund ist es ein sehr
charakteristisches Zeigermineral für Kobaltagerstätten, so dass
man es zur Prospektion von Lagerstätten verwendet. Die Halden und
die natürlichen Ausbisse der Erzgänge sind heute der Quell für die
hohen As-Gehalte in den Bächen, wie z. B. dem Schwarzbach im
Naturschutzgebiet vom Lochborn bei Bieber.

Silbriger, Bruchteile eines mm dünner Belag (Spiegel) aus Gediegen
Arsen auf dem Rhyolith von Sailauf (Bildbreite 2 cm,
gefunden 2012); in dieser Form ist es sehr selten - nicht zu
verwechseln mit den sehr ähnlich aussehenden Belägen aus
Manganoxiden. Das es solche Bildungen in der Natur gibt, spricht
für sehr außergewöhnliche Bedingungen, die zur Abscheidung von As
führen und in der Natur sehr selten verwirklicht wurden.
Das metallische Arsen als Elementmineral (ged. Arsen) entspricht
der Modifikation des roten Phosphors; Arsen kommt wie Phosphor als
Element in verschiedenen Formen vor, die völlig unterschiedliche
Eigenschaften aufweisen. Das Arsen in dieser Modifikation ist
pardoxerweise nicht giftig, da es im menschlichen Körper
weitgehend unlöslich ist. Und kein Mensch würde freiwillig das
Arsen in dieser Form essen, da es auch kaum als solches erhältlich
ist (auch auf den Münchner Mineralientagen 2013 wurden exotische
Elemente von der schweizer Fa. CristalTech in hochreinen, kleinen
Proben angeboten, aber kein Arsen; Begründung war, dass man das
Metall leicht ins Oxid überführen könne). Im Bergbau der
klassischen Erzregionen wurden die großen Massen als
"Scherbenkobalt" bezeichnet und zum Oxid verarbeitet.
Beispielsweise kam es in den Vogesen in so großen Massen vor, dass
man ganze Bergwerke danach betrieb und auch so benannte:
Giftgrube. Die seit langem bestehenden öffentlichen
Mineraliensammlungen legen Zeugnis ab von den unvorstellbaren
Mengen, die hier abgebaut wurden. Heute verwendet man metallisches
Arsen z. B. als unersetzlicher Legierungsberstandteil für
Lagermetalle in Gleitlagern.
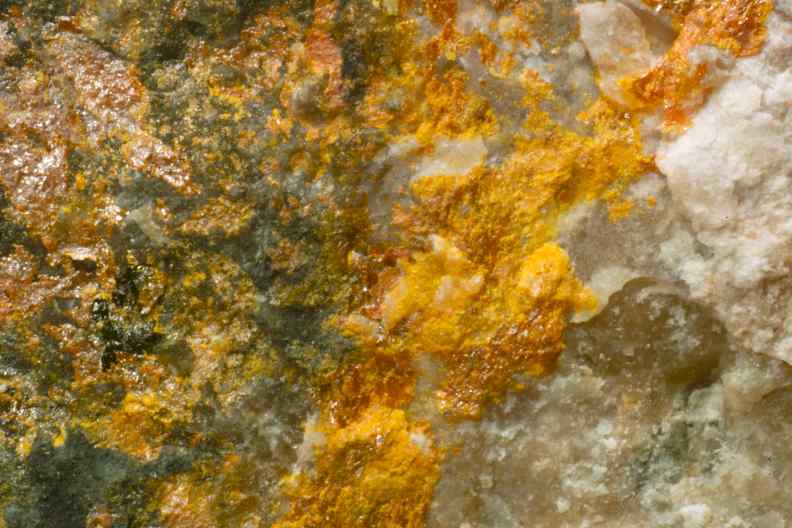
Orangener Realgar (α-As4S4, mit ca.
70% As) zusammen mit Illit als hauchdünne Kruste, die relativ lose
auf dem Rhyolith aufliegt, Bildbreite 5 mm. Diese winzigen Beläge
halten einer mechanischen Belastung kaum stand und regnen oft
schon ab. Die Verbindung ist aus vielen Erzvorkommen bekannt und
kommt auch in den Ablagerungen von Geysiren der Thermalgebiete
rezenter Vulkane vor. Realgar aus manchen Vorkommen ist nicht
langzeitsstabil und zerfällt in ein gelbes Pulver, aber nicht zum
gelben Auripigment.
Trotz des hohen Arsengehalts ist die Verbindung nicht giftig! Sie
ist recht stabil und war bereits im Altertum bekannt. Man pulverte
das Arsensulfid und stellte daraus sehr gute Farben her, die auch
in der Kosmetik Verwendung fanden. Auch das im Orient als
Enthaarungsmittel verwandte "Rhusma" wird aus Arsensulfid und
gebranntem Kalk (CaO) hergestellt. Weiter wurde das Material dem
Glas zugesetzt, gepulvert als geschätzte Malerfarbe und zum Färben
von Wachs verwandt. Die Verbindung ist als stabiles Farbpigment im
Sortiment und in guter Qualität nach wie vor im Farbenhandel zu
kaufen - ob das nach REACH noch noch sein wird, halte ich für sehr
fraglich.

Blaugraue, metallische Aggregate von Koutekit (eine sehr
seltene, intermetallische Verbindung Cu5As2
mit 32 % Arsen, Bildbreite 5 mm) mit Domeykit und gediegen Kupfer
in einer Kluft im Pegmatit. Diese winzigen Spuren in den
matamorphen Gesteinen zeigen eindrucksvoll die intensive
Durchdringung der spessarter Gesteine mit den erzbringenden
Fluiden auch abseits der großen und über km streichenden
Gangzonen. Dass es zur Bildung solch extrem seltener Phasen kam,
zeigt die ungewöhnliche Zusammensetzung der Fluide, die in kein
weit verbreitetes Schema passt. Bei einer gesamten Betrachtung
würden diese Spuren - für das bloße Auge an der
Sichtbarkeitsgrenze liegend - kaum etwas zum flächigen Arsengehalt
beitragen; diese Einschlüsse sind einfach zu selten. Aber würde
man bei einer Analyse zufällig solch eine Partie beproben, so
waren hohe As- und Cu-Gehalte die Folge.

Heller, körniger Pyrit im gelben Chalkoyprit mit
beginnender Verdrängung durch andere Kupfersulfide (Erzanschliff
aus Huckelheim; Bildbreite 2 cm). Der hellgelblich glänzende Pyrit
besteht im Idealfall ausschließlich aus Eisen und Schwefel (FeS2).
Solche Sulfide aus hydrothermalen Systemen enthalten aber immer
viele Spurenelemente, wie z. B. Arsen - im Mittel etwa 1.300 ppm,
was 0,13 % entspricht (Durchschnittswert aus 1.500 Analysen
(RICKARD et. al. 2017:121). Zu den begehrten Spurenelementen
gehören weiter Ni, Co und - Au!

Sogar das natürliche Arsenoxid (Arsenik) kommt im Spessart in
Spuren vor: Farblose, oktaedrische Kristalle als glitzernder Rasen
des seltenen Minerals Arsenolith (As2O3
mit 76 % Arsen, Bildbreite 5 mm). Von dem natürlichen Verbindung
gibt es auch noch eine monokline Form, die dann als Claudetit
bezeihnet wird - diese ist aus dem Spessart nicht bekannt. Der
erste Mensch, der das giftige Mineral im Spessart bei Bieber
nachwies, war der hanauer Chemiker Johann Heinrich KOPP, der
darüber schon 1807 berichtete: "Ueber den zu Bieber im Hanauischen
einbrechenden Kobaltvitriol und das ihn begleitende Arsenikoxyd"
im damals gerade neu begründeten Taschenbuch für die gesammte
Mineralogie, mit Hinsicht auf die neuensten Entdeckungen, heraus
gegeben von dem Mineralogen Carl Caesar von LEONHARD, ebenfalls
aus Hanau stammend. Im Stil der Zeit beschreibt er neben den
üblichen Eigenschaften, auch den Geschmack der Verbindung als
"zusammenziehend". Da er später noch Beiträge verfasste, hat er
die Geschmacksprüfung wohl überlebt.

Die Seiten 104 - 105 aus dem Taschenbuch für die gesammte
Mineralogie, mit Hinsicht auf die neuensten
Entdeckungen, 1. Band, erschienen 1807. In dem gleichen Beitrag
wird das später als Bieberit benannte
Kobaltsulfat beschrieben.

Als "Arsenikblüthe" beschreibt der Hanauer Mineraloge Karl Caesar
Ritter von
LEONHARD in seiner Oryktognosie von 1833 auf Seite 166 das
Arsenoxid;
man bachte, dass auch hier noch der Geschmack angeführt wird. Als
Vorkommen
wird auch Bieber im Hanauischen aufgelistet.
Toxische Mineralien sind in der Natur eigentlich selten. Von den ca. 5.500 verschiedenen, weltweit vorkommenden Mineralien (davon enthalten etwa 550 Mineralienarten Arsen in nennenswerten Mengen) gelten etwa 200 als potentiell gesundheitsschädlich bis giftig (die Diskrepanz zu den arsenhaltigen ergibt sich daraus, dass manche so selten sind oder das As so gebunden ist, dass es nicht löslich ist). Selbst Eisensulfate und Cobaltphasen sind in Grammmengen tödlich und selbst Calcit gilt als toxisch, da man sich mit Calciuim-Ionen auch vergiften kann. Als lethale Dosis für einen Menschen mit 70 kg werden 350 g Calcium angegeben (PUFFER 1980).
Mineralien, die einerseits wirklich als akut giftig gelten müssen und die auch in entsprechenden Mengen vorkommen, sind sicher selten - vielleicht kann man die an einer Hand abzählen. Außerhalb der Geowissenschaftler wird kaum jemand damit Kontakt haben können. Als Ausnahmen können die Mineralienbörsen angesehen werden. Aber hier ist der Preis der Schutz; es ist kaum vorstellbar, dass jemand hochpreisige Mineralien unsachgemäß behandelt. Arsenolith wird - wenn überhaupt - nahezu ausschließlich in µg- und mg-Mengen angeboten.
Fazit
Das Arsen ist ein ubiqitäres Spurenelement. Auch wenn es
schwer fällt zu akzeptieren, es ist natürlicher Bestandteil
unserer Umwelt und kommt überall vor - es ist immer eine Frage
der Art und dann noch eine der Konzentration. Erst die
gedankliche Assoziation mit dem Gift macht es zu einem
Problem.
Das über den Durchschnittsgehalten liegende Arsen in den
Felsen und Böden des Spessarts ist eine geogene Besonderheit,
von denen es in Deutschland noch einige weitere Beispiele, wie
den Bergbaugebieten des Harzes, des Erzgebirges, des
Schwarzwaldes, den Vogesen usw. gibt. Die landwirtschaftliche
Nutzung hat trotzdem hier Jahrhunderte lang statt gefunden und
man hat davon nichts gewusst. Es sind keine Schäden beschrieben
worden.
Das Trinkwasser im Spessart wurde erst "auffällig", als Europa
die Grenzwerte senkte - der Gewinn an Sicherheit ist aber damit
nur akademisch nachzuweisen.
Es ist im Spessart kein Fluch - es ist halt da.
Wirklich gefährlich wird es
ausschließlich dort, wo die Gehalte an leicht mobilisierbarem
Arsen in saurer Umgebung die %-Gehalte im Boden erreichen.
Nach meinem Kenntnisstand ist das ausschließlich im Raum
Bieber der Fall, wo auf einigen alten Halden des Bergbaues der
Pflanzenwuchs sichtbar gestört oder gar nicht mehr möglich ist
(hier spielen sicher weitere Schwermetalle wie Nickel, Kobalt,
Kupfer, Bismut usw. eine additive Rolle).
Weil in der Hartkoppe bei Sailauf die Besonderheit besteht, dass mit den As auch Uranyl-Ionen frei werden, die sich dann im Steinbruch-Regenwasser wieder finden, sei der Hinweis gestattet, dass es beim Uran ungleich komplexer ist. Hier kommt neben der toxikologischen Kompenente noch die der ionisierende Strahlung hinzu, die zwar bei der Allgemeinheit hoch bewertet wird, aber bei den Spurenstoffen keine nennenswerte Rolle spielt. Auch hier es so, dass eine geogene Anomalie vorliegt, die zu Spurengehalten im Wasser führt. Es wird aus egoistisch-politischen Gründen zum Problem gemacht.


Historische Apotheke im Spessartmuseum in Lohr. Die Apotheken (und
später auch die Drogerien) hatten
früher die Funktion einer Chemikalienhandlung, in denen man auch
alle Arten von Gifte kaufen konnte,
darunter auch Arsenik als Insektengift, wie in der alten
Glasflasche (ca. 1 l Inhalt) mit der Aufschrift
"Insektenpulver" rechts;
aufgenommen am 26.12.2005.



Historische Stufe aus Gediegen Arsen (metallisches
Arsen) aus Markirch, Elsass (Frankreich),
Bildbreite 7 cm
Kristallaggregate aus gedigen Arsen aus einem marinen Tonstein
nahe eines
Vulkans, gefunden beim Dorf Akadani, im Kreis Ohno der Echizen
Provinz
an der Westküste von Japan (HINTZE 1904:108f). Der Fund und Import
erfolgte durch die Kaiserlich Deutsche geologische
Japan-Expedition kurz
nach 1871, dann im Bestand der königlich sächsischen
Mineralien-Niederlage
in Freiberg.
Bildbreite 2 cm
Natives Arsen kommt in hydrothermalen Gangsystemen der
Wismut-Kobalt-Nickel-Abfolge auch in der elemantaren, metallischen
Form als graues Arsen vor (WEINER & HOCHLEITNER 1983:6f).
Besonders in den Vogesen wurde es beim Abbau auf Silber in großen
Mengen mitgewonnen und zu Fliegengift verarbeitet. Das hier
gezeigte Stück besteht fast ausschließlich aus dem Element Arsen,
mit einem alten Sammlungszettel der heute noch bestehenden Fa.
Krantz in Bonn, gefunden wahrscheinlich vor 1900 in Markirch
(heute Ste-Marie-aux-Mines) im Elsass (Alsace), Frankreich. Es
sind von hier massive Stücke mit 20 x 20 cm Größe bekannt
(MARTRAUD 2013:80ff). Diese sind bergfrisch metallisch grau und
laufen nach kurzer Zeit, so dass der metallische Charakter
verschwindet, so dass die älteren Belegstücke in den Sammlungen
unscheinbar grauschwarz aussehen. Sie sind mit einem Überzug aus
neu gebildetem Arsenolith überkrustet.
Bis 1940 wurde auf der berühmten Grube Gabe Gottes bei Markirch
das gediegen Arsen als Haupterz für die Herstellung von Rattengift
abgebaut. In fast allen Sammlungen der Welt finden sich Brocken
aus gediegen Arsen von dort. Unter Tage wurden Teile der
Gangmineralisation auch als Versatz gestapelt. Die daraus gelösten
As-Ionen führten zur Bildung einer ungewöhnlichen Vielfalt von
Arsenaten wie Pharmakolith, Haidingerit, Weilit, Fluckit,
Phaunouxit, Rösslerit, Hörnesit, Rauenthalit, Ferrarisit,
Guerinit, usw. in sehr attraktiven Kristallen und Aggregaten (BARI
1983:16, 18, 37). Hier wird auch sehr detailliert der Prozess aus
Oxidation und Neubildung der Arsenate beschrieben.
Auch aus dem Schwarzwald sind solche Gangmineralisationen mit
großen Massen an gediegen Arsen bescherieben worden. Bekannt wurde
neben den Gruben im Teufelsgrund, Herrenwald und die in den 1970er
Jahren nochmals aufgewältigte "Giftgtube" im Kaltwasser im
Münstertal. Hier wurde Gediegen Arsen als "Scherbenkobalt" in
einem Siderit-Gang gefunden und wohl im 18. Jahrhundert abgebaut.
Die untertägigen Teile der Grube sind nicht mehr zugänglich (MARKL
2017:96ff und 140ff).

In SCHUBERT´s Naturgeschichte von 1888 sind in der 3. Abt. 1. Teil
der illustrierten Mineralogie auf
Tafel 24 zahlreiche Arsenmineralien farbig abgebildet: ged. Arsen,
Auripigment, Realgar, Arsenopyrit
("Mißpickel"), Arsenolith ("Arsenit") und Pharmakolith.

Weißer Arsenolith als Resublimationsprodukt vom Gelände der
Muldenhütten,
Freiberg i. Sachsen, nachdem über den Haldenkörper mit ged. Arsen
glutflüssige Schlacke gekippt wurde, die das As angezündet hatte.
Die
As-Schwaden bildeten dann in den kühlen Bereichen einen
kristallinen
Niederschlag in kg-Mengen,
Bildbreite 6 cm.
Arsen ist in natürlichen Systemen überall vorhanden. Und man
findet es in Mineralien, in denen es eigentlich gar nich sein
sollte. So ist selbst im Quarz (Bergkristall; SiO2)
immer etwas Arsen enthalten. Die Gehalte liegen zwischen 0,4 und
5,2 µg/g. Selbst eine "High purity silica" ethält noch 0,18 µg/g
Arsen (BLANKENBURG 1994:72ff).
Nun gibt es natürliche Quellen, bei denen das Wasser lange unterwegs ist und dazu noch warm oder gar heiß. So in Wiesbaden, wo mitten in der Innenstadt heiße Quellen austreten. Am Kochbrunnen sind es bis zu 10 Liter pro Sekunde bei 67° C; wenn man mit konservativen 5 l/s rechnet, dann sind das 160.000 m³ pro Jahr; alle Quellfassungen im Stadtgebiet summieren sich auf ~725.000 m³! Darin gelöst sind ungefähr 5.500 t Kochsalz. Der Arsengehalt liegt bei 100 µg/l, was sich zu einer Arsenförderung von etwa 14 t pro Jahr multipliziert (STENGEL-RUTKOWSKI 2009:4ff). Diese und die anderen Quellen im Wiesbadener Untergrund reicherten das Arsen im Untergrund an, so dass man heute Werte von 130 mg bis zu 3 g/kg nachweisen kann. Hinzu kommt Thallium mit 250 mg/kg, was ebenfalls als bedenklich eingestuft wird. Nun ist 2021 der neue Taunus-Führer aus der renommierten Reihe der Sammlung Geologischer Führer Band 111 erschienen (ANDERLE et al. 2021). Dabei muss man sich fragen, ob eine "Arsenphobie" inzwischen auch die Geologen erreicht hat, denn auf S. 93 Tab. 5 sind alle Inhaltsstoffe und Eigenschaften des Wiesbadener Thermalwassers aufgelistet, aber eben kein Arsen, obwohl es in der zitierten Quelle angegebenen ist! Immerhin war der in der 1980er Jahren deswegen abgedeckt worden, weil man darin eine Gefahr sah.
Wissenswertes zum Arsen
Zusammen mit Quecksilber, Thallium, Blei und Antimon gehört Arsen
zu den Schwermetallen aus der dunklen Seite des Periodensystems.


Links: Leuchtend rote, in frei stehende Kristalle aus Realgar
(α-As4S4) auf weißem Calcit von der Shimen
Mine, Changde Präfektur, Huan Provinz,
China, Museum für Naturkunde Berlin, Nr. 1997-0136. In der Natur
kommt das Tetraarsentetrasulfid in 3 verschiedenen kristallinen
Formen vor:
Realgar, Pararealgar und Bonazziit.
Bildbreite ca. 13 cm.
Rechts: Großes Spaltstück eines durchsichtigen Auripigment (As2S3)
aus der Tong-Ren-Mine in China
Bildbreite 7 cm.
Arsen ist als schädliche Noxe lange bekannt und die ersten
Erfahrungen kommen aus dem Bergbau und der Hüttentechnik der
Antike. Man verarbeitete insbesondere die auffallenden Mineralien
Realgar und Auripigment; einerseits zu einem Farbpigment und
nebenbei auch zu Arsenik. Künstlicher Realgar ist beispielweise in
der Friedrichs-Hütte von Richelsdorf (Hessen) in blättrigen
Aggregaten als Hüttenprodukt aufgetreten (LEONHARD 1846:69).
Ausstellung zum Fund der weltberühmten, ägyptischen Büste Nofretete in Berlin 2013:
In einer etwa 9 x 9 cm großen, flachen Pappschachtel lag ein etwa dreieckiges Stück schwefelgelben Auripigments (ähnlich der Abbildung oben rechts; man beachte den selbst erklärenden Namen aus lat. aurum für Gold und pigmentum für Pigment! (CACARASSO & LINIAN 2013:73ff). Das an der Kathete ca. 7 cm lange und ca. 1,5 cm dicke, plattige Stück ist an der stumpfen Oberfläche abgenutzt, als hätte man es zum Kreiden genommen. Nur an einer Stelle ist ein ca. 7 mm großer Ausbruch zu sehen, der die typische Spaltbarkeit und Farbe des Minerals erkennen lässt. Der darunter liegende, gebräunte Papierzettel trägt die Nummer 37276 und oben die Aufschrift "Auripigment". Das Stück war ohne weitere Beschriftung in einer flachen Vitrine zusammen mit weiteren Pigmenten in der Ausstellung "Im Licht von Amarna. 100 Jahre Fund der (Büste) Nofretete" in Tell `Amarna (Ägypten) in Berlin zu sehen. Aus dem Fundzusammmenhang lässt sich schließen, dass das wahrscheinlich zur Pigmentgewinnung verwandte Stück Auripgment aus der Zeit um etwa 1.350 v. Chr. stammt. Ob es wirklich Auripigment oder ein ähnliches Arsensulfid ist, ließe sich nur nach einer röntgendiffraktometrischen Untersuchung sagen. Das bemerkenswerte Ausstellungsstück ist nicht im umfangreichen Katalog der Ausstellung abgebildet und auch dort nicht beschrieben (infolge des unverständlichen Fotografierverbots kann hier nur eine Beschreibung wieder gegeben werden).
Gelborangener Auripigment kann in Bergwerken in unvorstellbaren
Mengen auftreten. So berichten KLEINE et al (2014) über den Fund
von wunderschönen Auripigment-Kristallen in dem
Twin-Creeks-Tagebau in Nevada (USA), wo eine
Carlin-Typ-Lagerstätte auf Gold abgebaut wird (bei diesem
Lagerstätten-Typ ist das Gold mit dem bloßen Auge nicht sichtbar;
die Mine produziert ca. 28 t Au pro Jahr). In den Jahren 1999 und
2000 wurden in Drusenhohlräumen tausende von Stufen mit
wunderschön glänzenden, bis zu mehrere cm-große
Auripigment-Kirstallen professionell geborgen und dem
Mineralienmarkt zugeführt. Den Fotos in dem Beitrag kann man
entnehmen, dass hier im Fels tausende von Tonnen Auripigment
anstanden, die schließlich für die Goldgewinnung verarbeitet
wurden. Es gibt auch in diesem Vorkommen eine deutliche Affinität
zwischen dem Vorkommen von Arsen und Gold - wie an anderen Orten
auch.


Zitronengelber Auripigment als dünne Kluftbeläge mit weißem Calcit
in einem dolomitischen Gutensteiner Kalk (Plattenkalke der
ladinischen
Partnach-Formation) vom Dielengraben bei Stein bei Dellach in
Kärnten (Österreich), gefunden vor 1975,
Bildbreite links 12 cm, rechts im Ausschnitt 5 mm
Beim händischen Abbau wurden sicher relativ hohe Dosen an Staub eingeatmet, der zusammen mit dem verbreiteten Quarz und örtlich noch Radon zu Lungenkrankheiten geführt hat. Mit Beginn der Bohr- und Sprengtechnik wurden die Belastungen noch höher, weil man zunächst nur trocken bohrte und dabei sehr viel Staub erzeugte (heute wird nass gebohrt, um den Staub zu binden).
Die frühen Alchemisten kannten das Arsenik und bei den Versuchen
wurde entdeckt, dass man damit Metalle - wie z. B. Kupfer -
aufhellen konnte. Dies ging auch beim Zinn, so dass man ein Metall
mit silberähnlichem Aussehen erzeugen konnte; es konnte aber nicht
für Speisen oder Getränke verwandt werden. Auch als Stoff zu
Gerben ließ sich Arsenik verwenden; dies wurde insbesondere in
Venedig angewandt, wo man unter zu Hilfe nahme von Schwefel und
Arsen ein goldenes und silbernes Leder herstellen konnte.
Den mengenmäßig größten Bedarf hatten die Glashütten, die dem
Gemenge bis zu 10 % Arsenoxid (arsinico) zusetzten um damit ein
erstklassiges, farbloses und klares Glas zu erhalten. Diese
Entdeckung ging von Venedig aus und wurde durch Wissenstransfer in
ganz Europa angewandt. Die Glasfabrikation von Murano verbrauchte
1868/69 in 44 Wochen 124 t Arsenik! Das bedeutet, dass all die
Gläser aus dieser Zeit deutlichen Arsengehalte aufweisen (ALLESCH
1959).
Im Märchen Schneewittchen wird ein vergifterer Apfel als Mittel
zur Tötung eingesetzt; auch wenn die Gebrüder GRIMM nicht explizit
Arsen(ik) erwähnen, kann man aufgrund der Entstehungszeit Ende des
18. Jahrhunderts vermuten, dass man hier auch Arsenik meinte,
welches dem Apfel zugesetzt wurde.
Weite Verbreitung erlangte Arsen im 19. Jahrhundert als
faszinierend intensive grüne Farbe für Malerfarbe, Tapeten,
Stoffdrucke und Blumenschmuck. Dafür wurde ein Kupferarsenitacetat
(Cu(CH3COO)2 • 3Cu(AsO2)2,
Scheel´s oder Schweinfurter Grün) und Kupfer(II)-Acetoarsenit
(Pariser Grün) in großen Mengen als leuchtend smaragdgrünes
Pigment hergestellt (in Deutschland wurde die Verwendung ab 1882
verboten) und nach dem Färben von Hand weiter verarbeitet; die
Verbindungen sind nicht sehr stabil, so dass das Arsen auch ohne
Zutun - auch als Gas frei werden kann. Dies geschah wohl bei
erhöhter Feuchtigkeit, wohl mit Hilfe von Pilzen (sogn.
"Arsenpilze" wie beispielsweise Scopulariopsis brevicaulis;
übrigens kann der auch als "Fußpilz" weiter getragen werden)
oder/und Bakterien wurden erhebliche Mengen des sehr giftigen
Arsenwasserstoffs (Arsin AsH3) und Trimethylarsin (CH3)3As)
als Gas frei gesetzt, was zu einem bekannt knoblauchartigen Geruch
führte. Übrigens ist das Grund für den Namen der Farbe als
„Giftgrün“!
Man verwandte eine Mischung aus gepulvertem Arsenik, Seife, Salz,
Kaliumcarbonat, Kampher und Kalk zur dauerhaften Präparation von
Tierbälgen für die naturwissenschaftlichen Sammlungen und Museen
der Welt (auch viele der Präparate im Naturwissenschaftlichen
Museum der Stadt Aschaffenburg wurden mit Arsenik dauerhaft gegen
Schadinsekten geschützt). Auch der Teer für den Anstrich von
Schiffen wurde mit Arsenik angereichert, um den Organismen
("Schiffsbohrwurm", eine Muschel im Salzwasser, die Holz verdauen
kann) des Zerstören des Holzes der Schiffe zu erschweren.
Im Bürgerkrieg der Vereinigten Staaten von Amerika wurden Menschen
mit Arsenik einbalsamiert und so deren Leichen haltbar gemacht;
man hatte das Verfahren entwickelt, nachdem aufgefallen war, dass
Leichen nach Arsenvergiftungen wesentlich langsamer verwesen als
normale Leichen. Noch im frühen 18. Jahrhundert wurde in London
sogar Wein mit Arsensalzen "verbessert"!

Arsensäure (Acid. arsenicos.) als weißes
Pulver in einer Glasflasche von ca. 50 ml
Inhalt, ausgestellt im Apothekenmuseum
im Schloss in Heidelberg.
Der schlechte Ruf von "Arsen" und die Assoziation mit dem Gift
schlechthin hat seinen Ursprung im viktorianischen England des 19.
Jahrhunderts (Arsen als halbmetallisches Element ist nicht giftig,
da es menschlichen Körper bei einer oralen Aufnahme infolge der
kurzen Verweilzeit kaum gelöst wird).
Wurde Arsen als Gift verwandt, so kann man es nach Jahrhunderten
noch nachweisen. So wurden im Grab des Francesco I. (1541-1587)
aus der Dynastie der Medici Gewebereste gefunden, die noch
Arsen enthalten haben, so dass man davon ausgehen muss, dass der
Mann von Ferdinando I. (1549-1609) aus dem gleichen Geschlecht
vergiftet wurde (Anonym 2013:68). Aus den Erfahrungen reifte auch
die Notwendigkeit, sich gegen das Gift zu schützen. Neben
zahlreichen Verfahren der Hilfe vom Beten bis zum Vorkoster, gab
es einen reichen Glauben an die schützende Wirkung von - aus unser
heutigen Sicht - absonderlichen Ritualen. So wurde beispielsweise
dem Bezoar, einem Konkrement aus dem Magen von Widerkäuern eine
solche Wirkung zugesprochen und solche Gebilde von ansehnlicher
Größe zu allerlei Produkten verarbeitet (DO SAMEIRO BARROSO
2013).
RÖßLERN (1700: 157ff) berichtet in dem Kapitel "Von dem Arsenico,
wie derselbe gemacht wird" wie man den Rauch beim Rösten
gefangen werden muss. Das Resublimationsprodukt aus Kiesen und den
"wilden Erzen" wird Arsenico oder Mehl beschrieben. Die Personen
tragen beim Herauskratzen des [Gift-]Mehls aus den Rauchfängen
(hier als Gewölbe bezeichnet) einen die Nase und Maul verbindenden
Mundschutz (auf der Abb. gegenüber dargestellt). Sie sollen vorher
etwas Speck gegessen haben. Das hat seinen Grund darin, dass das
Arsenic in Wasser (Speichel bzw. Mund- oder Nasenschleimhäute) gut
löslich, aber in Fett kaum löslich ist. Es ist eine frühe Form des
Arbeitsschutzes. Trotzdem dürfte die Aufnahme des Staubes so hoch
gewesen sein, dass den Hüttenleuten kan langes Leben beschieden
war.

Oktaedrische, farblose Arsenolith-Kristalle (Arsenik) aus einer
brennenden
Kohlehalde von La Ricamarie, Loire, Rhone-Alpes, Frankreich.
Bildbreite 2 cm
Das Arsen wird bei der Verbrennung von Kohle frei und resublimiert
an
der kälteren Oberfläche als Arsenik - wie in einem Schornstein.
Die Verwendung des Oxids als Gift für Menschen war sicher bereits in der Antike bekannt, kam aber erst in de Neuzeit aus Italien über Frankreich nach England. Die Erzbergwerke in Großbritannien förderten sehr große Mengen an Arsen reichen Erzen, die in den meist nahe bei den Gruben gelegenen Aufbereitungen verarbeitet wurden (1870 wurde aus der englischen Grube Devon Great Consols aus dem dort anstehenden Arsenopyrit die Hälfte des Weltbedarfs an Arsen gedeckt!). Dabei kam das Rösten der Erze unter Sauerstoffüberschuss zum Einsatz. Die Gase wurden über lange Zuleitungen zum Abkühlen an die Schornsteine geleitet (KARSTEN 1831:567ff). Hier kondensierte und sublimierte ein Teil der flüchtigen Bestandteile, darunter auch das Arsenoxid (genau Diarsentrioxid As2O3, besser bekannt als Arsenik) als weißer Belag an den Wänden. Arbeiter kratzten dann die Beläge ab und dieses wurde als Gift verkauft. Auf alten Fotos kann man Arbeiter sehen, die die weißen Sublimate aus den Essen mit Sandschaufeln in hölzerne Schubkarren schippen und als einzigen Atemschutz Baumwollflocken in der Nase tragen (BANCROFT & WELLER 1993:267 fig. 9)!
Es gab bereits im 13. Jahrhundert Bergwerke in Sachsen (u. a. Freiberg), die die Gewinnung des Hüttenrauchs zur Produktion von Arsenik nutzten. Das Verfahren wurde dann nach Österreich exportiert, wo man im alpinen Raum seit dem späten 14. Jahrhundert zahlreiche Bergwerke betrieb, die vorwiegend Arsenopyrit gewannen, aus dem das Arsenik aus dem Hüttenrauch gewonnen wurde. Das Produkt wurde dort mundartlich als Hüttrauch, Hüttrach, Hittrach oder so ähnlich bezeichnet. Das teils noch reffinierte Material wurde bis nach Venedig, aber auch nach Deutschland verkauft. 1870 erzeugten 8 Arbeiter in dem Arsenikwerk Rothgülden nahezu 22 t Arsenik (pro Jahr)! Die Konkurrenz ab dem 18. Jahrhundert war eine enorme Arsenikproduktion in Reichenstein in Niederschlesien (heute Zloty Stok in Polen, dort wurde die Arsenikproduktion erst 1961 eingestellt), welche über Meißen in Sachsen verhandelt wurde. Von hier aus wurde das Arsenik über die Elbe kostengünstig bis in den Mittelmeerraum transportiert und machte den ostalpinen Produzenten erhebliche Konkurrenz (ALLESCH 1959).
Diese pulrigen Niederschläge der Rauchfänge wurden dann entweder raffiniert oder direkt verkauft. Der Preis dafür war sehr niedrig. Das Arsenik war lange Zeit frei verkäuflich, denn man verwandte es in den Haushalten als Fliegen-, Mäuse- und Rattengift. Als Insektenvertilgungsmittel wurden hohe Dosen von Arsenverbindungen bis zur Einführung des DDT in vielen angelsächsischen Regionen verwandt; auf diesem Weg gelangten dann auch nennenswert Mengen in die Nahrungsmittel für Menschen. Bis 1999 wurde der Nahrung von Hühnern als Wachstumsförderer die ungiftige 3-Nitro-4-Hydroxyphenylarsonsäure (Roxarson) in Spuren beigemischt. Als Holzschutzmittel, z. B. für Telegraphenmasten, verwendet man u. a. ein Chromat-haltiges Kupferarsenat (CCA) mit dem Markennamen Ascu, in der EU seit 2002 verboten. Es wird unter Druck zum Imprägnieren des Holzes verwandt. Als Medikament sind Arsenverbindungen weltweit seit Langem in Verwendung; bekannte Beispiele sind die FOWLER´sche Lösung (Kaliumarsenit in Lavendelwasser zur Odorierung bis ins 20. Jahrhundert angewandt) von Thomas FOWLER und das berühmte Medikament Salvarsan von Paul EHRLICH. Weiter sind bekannt Atoxyl, Tryparsamid und Maelarsoprol. Heute wird Trisenox auf der Basis von Arsenik zur Behandlung einer seltenen Form von Leukämie angewandt (ROTH 2013:196). Und in der Homöopathie wird Arsen immer noch verwandt, wenn auch in einer so großen Verdünnung, dass sich so gut wie kein As mehr in der Lösung befindet.

Die Arsenoxide kommen in der Natur auch in größeren Mengen vor.
Links
Claudetit und rechts ein großes Stück Arsenolith in der
Schausammlung
des Museums für Naturkunde, Berlin.
Der berühmte Goldbergbau zwischen Rauris und Bad Gastein in den
Hohen Tauern Österreichs konnte in der vorletzten Abbauperiode nur
betrieben werden, weil man das Arsen aus dem Arsenkies röstete und
von dem Erlös die Kosten des Bergwerks bestreiten konnte. Dazu hat
das Gold und Silber nicht ausgereicht. Von 1917 bis 1926
produzierte man 746 t Arsen. Man verwandte das Arsen als
Legierungsbestandteil für Schrapnellgeschosse (GRUBER 2016:27).

Fabrik zur Raffination des "Giftmehls" zu reinem Arsenik in den
Arsenwerken "Reicher Trost"
in Reichenstein in Schlesien (Złoty Stok, Polen). Man beachte die
Ausrüstung der Arbeiter
mit Handschuhen, einem Gesichtsschutz, der auch den Hals abdeckt,
Kappen und Schutzbrillen.
Dazu eine ganze Schubkarre mit Arsenik!
Abbildung aus KRAEMER (1906:173).
HELMUTH (1808:456) berichtet, dass die oben angeführte Hütte in
Reichenberg in Schlesien pro Jahr über 1.000 Zentner (also 50 t)
Arsenik gewinnt. Bei den "Steinen" in der Schubkarre und am Boden
handelt es sich um "Arsenikglas", welches in gusseisernen Kesseln
(im Hintergrund rechts) aus pulvrigem Arsenik erzeugt wird (LENZ
1856:291).
Eine Besonderheit waren die Arsenikesser in der Steiermark und
Tirols im 19. Jahrhundert, aber auch in Indien und den Südstaaten
der USA. Diese aßen steigende Dosen von Arsenik (und
Arsensulfiden) als Stimulanz; dabei konnte man die Dosis so lange
steigern, bis eine sonst lethale Dosis vertragen werden konnte.
Der Mechanismus der As-Aufnahme über den Verdauungstrakt ist nicht
geklärt.
Das Arsenik (und verschiedene Arsensulfide) wurde zur
Leistungssteigerung gegessen. Gleichzeitig ging damit eine
generelle Verbesserung des Aussehens und man konnte damit eine
Gewichtssteigerung einleiten, was in früheren Zeiten bei starker
körperlicher Arbeit erwünscht war. Wenn das Arsenik abgesetzt
wurde, traten Entzugserscheinungen wie bei einer Sucht auf, so
dass man das Arsenikessen mit dem heutigen Genuss von Extasy und
ähnlichen Drogen vergleichen kann. Die Verwendung zwischen
Eigenmedikation und Aphrodisiakum ist wohl fließend gewesen.
Infolge von Fehldosierungen gab es auch Todesfälle. Das Mittel
diente auch als "Roßarznei" zur Leistungssteigerung, aber auch zum
Schönen von Pferden (ALLESCH 1959, SUCHER 2011:59ff). Das Arsensik
wurde sogar als "Genussmittel" für Menschen angesehen, wenn auch
als merkwürdiges, so wie Thee, Kaffee, Coca, Chokolade, Haschisch,
Fliegenschwamm (von BIBRA 1855:381).

Arsensulfid in seiner schönsten Form: Rotorangene und
durchscheinende,
blockige Kristalle aus Auripigment aus der Quiruvilca Mine,
Santiago de
Chuco, La Libertad, Peru, Sammlung K. Müssig, Miltenberg,
Bildbreite 8 cm..
Das klassische Arsenik ist leicht in Wasser löslich und mit
anderen Stoffen geschmacklich einfach zu maskieren, so dass man es
nicht schmeckt. Und bis zur Mitte des 19. Jahrhunderts war die
chemische Wissenschaft noch nicht flächendeckend in der Lage, As
in Gewebeproben nachweisen zu können. Aus diesem Grund wurden aus
ganz verschiedenen Motiven zahlreiche Menschen damit vergiftet.
Die zunehmende Aufklärung solcher Verbrechen und deren Geschichte
wurde mit der Verbreitung von Tests (wie z. B. die Marsh- oder
später die Reinsch-Probe) veröffentlicht; darüber gibt es eine
große Zahl an Veröffentlichungen (WALTHER 1842). Sie bilden den
Hintergrund für die Stoffe, aus denen die vielen Kriminalromane
entstanden, deren Ruf bis heute eine sofortige Verknüpfung von
Arsen - egal in welcher Form - mit Arsenik hervor ruft. Man denkt
an das Arsen in den Kerzen (GRANVILLE. 1838), den grünen Tapeten
(HAWKSLEY 2018) oder vielen Vergiftungsfälle in den
Kriminalromanen von Agatha CHRISTIE, die mit nahezu
wissenschaftlicher Präzision die Umstände beschreibt. In
Deutschland wurden die Verfilmungen mit Margaret RUTHERFORD als
"Miss Marple" zu außergewöhnlichen Erfolgen. Oder Gustave
FLAUBERT´s "Madame Bovary" und Josef O. KESSELRING´s "Arsenic and
Old Lace" - zu deutsch "Arsen und Spitzenhäubchen", dessen
Verfilmung 1961 das Stück bekannt machte; es wird noch heute an
vielen Orten aufgeführt.
Und im nächsten gedanklichen Schritt wird aus dem Arsen nur noch
Mord durch Vergiften. Dies ist nahezu unauslöschlich in den
Gehirnen verankert und überall verbreitet. Eine rationale
Argumentation über unterschiedliche Toxidizität, Wertigkeiten,
Bindungen, Konzentrationen oder Lösungsvermögen ist sehr schwer
oder gegen eine existenzielle Angst fast unmöglich.
Ein wirkliches Problem sind die sauren Abwässer aus Halden der
alten Bergbauaktivtäten. Diese Wässer können erhebliche Frachten
an Arsenionen führen; oft dazu weitere Schwermetalle, die durch
das Zersetzen von Sulfiden als Sulfat ins Wasser gelangen. Je nach
dem Rest in dem Haldenkörper kann ein Teil fixiert werden, in dem
es zur Neubildung von unlöslichen oder schwer löslichen Mineralien
kommt (z. B. Jarosit). Wie neuere Experimente zeigen, kann das
Arsen mittels preiswerter Knochenkohle auch im großtechnischen
Maßstab fixiert werden (LIU et al. 2014).
Dies wird noch gestützt durch die Entwicklung von Kampfstoffen für
die chemische Kriegsführung auf der Basis von Arsen durch den
amerikanischen Chemiker Winfried Lee LEWIS:
Dichloro(2-Chlorovinyl)arsin, bekannt als "Lewisit". Da es sehr
empfindlich gegenüber Feuchtigkeit ist, wurde es praktisch nie
eingesetzt, nur Altlasten machen heute noch Probleme - aber eben
wieder Gift.

Zitronengelber Auripgiment mit Calcit aus der Shimen Mine, Changde
Präfektur, Huan Provinz, China, Sammlung K. Müssig, Miltenberg,
Bildbreite 8 cm.
Auf dem nahezu unüberschaubaren Markt der Schmucksteine finden
sich immer neue, meist schön farbige oder strukturierte Gesteine
und Mineralien. Das als "Eclipse" oder "Mustardjaspis" angebotene
Gestein besteht nach den Ausführungen von Bernhard BRUDER vom EPI
in Ohlsbach aus einem Kalkstein, in dem neben vulkanischer Asche
auch Auripigment und vermutlich elementarer Schwefel eingewachsen
ist. Infolge der geringen Härte wird bei der "Verwendung" leicht
Material aus der Oberfläche abgetragen oder infolge der geringen
Beständigkeit gelöst.
Es scheint auch hier so zu sein, dass je geringer die wirkliche Gefahr ist, um so größer ist die Angst davor: Der Bürger fürchtet sich vor einigen µg/kg Arsen - fährt aber ohne jede Bedenken einen PKW. In Deutschland stirbt niemand an Arsen, aber ca. 4.000 Menschen pro Jahr im Straßenverkehr und viele mehr tragen dauerhafte Schäden davon. Und auch die Medien machen sich diese irrationalen Ängste zu Nutze und schlachten solche vermeintlichen "Tatbestände" aus. Die Irreführung wird dann erhalten, in dem man einerseits keinen Messwert angibt, sondern die wievielfache Überschreitung eines Grenzwertes, dessen Größenordnung man nicht kennt und auch nicht nennt. Dass Analysenwerte auf Trockenmassen bezogen und die Fehlern behaftet sind, die bei niedrigen Konzentrationen erheblich sein können, wird einfach unterschlagen oder als bekannt vorausgesetzt. Weiter verzichtet man auf die Angabe von Vergleichswerten, so dass der veröffentlichte Wert isoliert im Raum steht. Infolge der leichten Nachweismöglichkeiten bis in den ppb-Bereich gibt es praktisch keine Stoffe, in dem man nicht irgendeine Verbindung nachweisen kann, die Besorgnisse erregen kann.
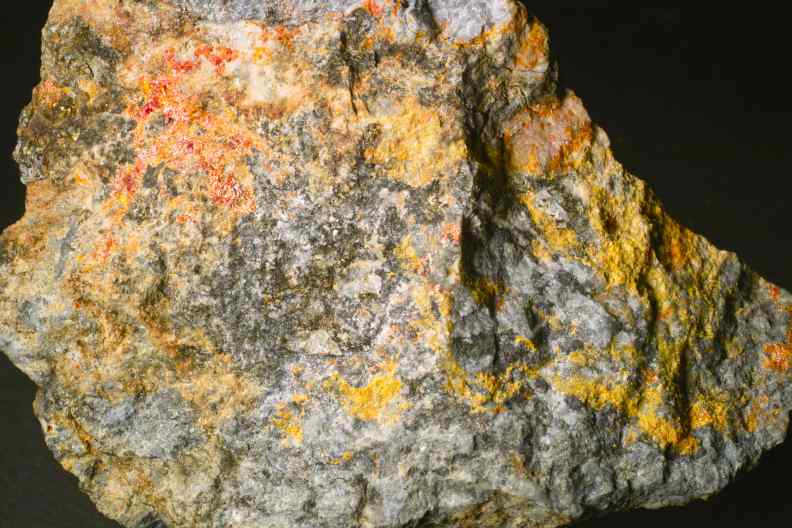
Aus der Lagerstätte von Cavnic bei Baja Mare in Rumänien stammt
dieses
Stück Quarz mit Realgar und Auripigment,
Bildbreite 7 cm.

Angelöste Arsenolith-Oktaeder auf angewittertem Gediegen Arsen aus
St.Marie-aux-Mines,
Bildbreite 1,5 mm
Die Akademisierung des Arbeitsschutzes dringt inzwischen auch
beim As in Regionen vor, bei denen man sich nur noch wundern kann.
Der AGS hat in seiner Frühjahrssitzung 2013 (KAHL 2013:17) als
Ergänzung des BekGS 910 die Toleranzkonzentration für anorganische
Arsenverbindungen auf 8,3 µg/m³ (E) in der Luft und den
Akzeptanzkonzentration auf 0,83 µg/m³ (E) bei einem
Überschreitungsfaktor von 8 festgeschrieben. Wenn man das
umrechnet, dann sind das 0,000.642 g/t As-Verbindungen in der
Luft. Damit dringt man sehr nahe an die ubiqitäre Grenzen des
natürlichen Auftretens vor. Weiter ist aber zu bezweifeln, dass
man diese Grenzwerte mit einem vertretbaren Aufwand überhaupt
sicher nachweisen und einhalten kann, da man sich ja im Bereich
von unter 1 Millionstel g/m³ bewegt; die Zweifel liegen nicht so
sehr beim analytischen Nachweis in der Probe, als denn bei der
Probennahme. Weiter wird dabei keine Rücksicht genommen, ob die
Substanz in der Lunge löslich ist oder nicht.
Beispiel gefällig?
Bei der Produktion von Gehörschutzstöpseln gegen den Lärm in Industriebetrieben aus einem geschlossen porigen Schaumstoff wird der gelbe und sich an die Ursprungsausdehnung erinnernde Kunststoff mit einer Antimonverbindung stabilisiert. Das Element Antimon ist dem Arsen chemisch sehr ähnlich, aber auch in seinen Verbindungen nicht giftig. In der Natur kommen die beiden Halbmetalle oft miteinander vor, so dass im Antimon oft auch etwas As nachweisbar ist - auch in den daraus hergestellten Produkten. Die Zeitschrift "Ökotest" (Juli 2002) kaufte in Apotheken Gehörschutzstöpsel, suchte nach Schwermetallen und fand Spuren von As. Die Dämmung gegen Lärm war nicht Gegenstand der Prüfung (sic!). Der Nachweis wurde dann begierig von den Medien aufgenommen und man lehnte die Stöpsel als "Gift" ab. Selbst die Gewerkschaft, die sonst sich für allwissend haltende IG Metall, sprang auf den gleichen Zug auf und glaubte, die Unternehmer "vergiften" die Mitarbeiter. Alle Dementi, auch seitens der Fachleute bei den Berufsgenossenschaften, halfen nichts. Dass man für eine Aufnahme des As die Stöpsel hätte essen müssen, wurde dabei vergessen. Diese Stöpsel steckt man sich ins Ohr, damit man vor dem gehörschädigenden Lärm vieler Industriebetriebe bzw. Arbeitsverfahren geschützt ist. Denn der Kontakt zwischen Stöpsel und Haut ist auf die schaumige Oberfläche von wenigen cm² beschränkt. Im Schaumstoff ist das As gebunden und diffundiert durch den Ohrschmalz nicht bis zur Haut. Da es in dem Umfeld Ohr nicht gelöst werden kann, kommt es nicht bis auf die Haut. Durch die Haut hätte das As dann auch noch gelangen müssen. Und für eine wirklich Vergiftung hätte man kiloweise Stöpsel essen müssen (ich kenne niemanden, der auch nur einen Stöpsel freiwillig oder versehentlich gegessen hat). Trotz allem wurden die Stöpsel nicht mehr verwendet und letztlich weggeworfen. Der namhafte Hersteller musste sein gutes und über viele Jahre von großen Mitarbeiterkreisen akzeptiertes Produkt umstellen und einen anderen Stabilisator verwenden - es dauerte Jahre, bis das mit dem Gift im Stöpsel vergessen war. Ob der jetzt verwandte Stabilisator für den Schaumstoff im Gehörgang besser ist, kann ich nicht sagen, da er mir nicht bekannt ist.
Ein Gewinn für die Sicherheit ist hier nicht erkennbar; im Gegenteil haben Menschen aus Angst vor dem Arsen die Stöpsel nicht benutzt und sich einen Schaden am Gehör zugezogen.
Die gleiche Systematik ist mit anderen Stoffen und den daraus
gemachten "Skandalen" bekannt. Aperiodisch werden solche Umstände
durch die Medien gepeitscht, bis nach ein paar Wochen das
Interesse daran erlahmt (Acrylamid kurz vor Weihnachten in den
Plätzchen, Dioxin(-äqivalente) in der Konzentration von wenigen pg
(in der Trockenmasse) in den Eiern bzw. im Tierfutter, ...). Eine
sehr lesenwerte Zusammenstellung und Bewertung findet man in dem
Werk von ROTH (2013). Der letzte zum republikgefährdenden Umstand
erhobene Skandal war das Fibronil in den Eiern im Sommer 2017.
Im Zusammenhang mit dem Fraking bei der Förderung von Erdgas
("Schiefergas") wird oft behauptet, dass das damit das Grundwasser
verseucht werden kann. Dabei wird oft vergessen, dass die Wässer
aus großen Tiefen von einigen km und daher mit hoher Temperatur
ein großes Lösungsvermögen besitzen und sehr viele gelöste Ionen
enthalten, die ein Trinken unmöglich machen. Aus geothermalen
Feldern des Yellowstone National Parks sind As-Gehalte von 100 bis
10.000 µg/l, aus den vulkanischen Thermalgebieten Neuseelands sind
230 - 6.500 µg/l und auch aus El Tatio in Chile werden 45.000 -
50.000 µg/l angegeben worden (BOWELL et al. 2014:6). Zur
Erinnerung: Der deutsche (europäische) Grenzwert für Trinkwasser
liegt bei 10 µg/l Arsen.
In Aschaffenburg ist die Verwendung von Schotter aus Sailauf zum Politikum geworden: Aus parteipolitischen Gründen
avanciert(e) der dauerhaft harte Rhyolith-Schotter zu
einem Problem für Kinder und wird unsachlich als "Gift"
bezeichnet. Arsen (As) ist in der Natur praktisch
überall vorhanden und mit durchschnittlich 1,7 Gramm pro
Tonne Bestandteil der Erdkruste. Die tatsächlichen
Gehalte unterliegen, je nach der Natur des Materials,
erheblichen Schwankungen. Die Gesteine des Spessarts und
des Odenwalds - und in vielen anderen Regionen auch -
enthalten immer Spuren von Arsen, in der Regel in
einigen µg/g, g/t oder ppm (parts per million - Teile
auf eine Million). Die modernen Analysenmethoden lassen
dies leicht und kostengünstig nachweisen. Eine
Gesundheitsgefahr geht davon keinesfalls aus, da man
Gesteine üblicherweise nicht isst (wenn man von
»Heilerde« absieht, aber da ist halt auch Arsen drin).
Es sterben sicher mehr Menschen durch Stolpern auf einem
Schotterweg als durch eine Spurenelementvergiftung mit
Arsen. Arsen - egal in welcher Konzentration - weckt
beim Menschen automatisch die Assoziationen zu den
historischen tödlichen Vergiftungsberichten, die durch
Diarsenpentoxid (Arsenik) hervorgerufen werden kann. Um
dies zu erreichen, müsste man einige Kilogramm Schotter
essen, was aufgrund der Härte ohne Zwang nicht geht. Und
selbst das würde nicht gehen, da das Arsen in dem
Schotter im Magen nicht löslich wäre. Also wird hier mit
einem Stoff, der selbst im Trinkwasser des Spessarts
(auch und gerade des Sandsteinspessarts) weit verbreitet
ist, die Angst geschürt, ohne dass es dafür eine
wirkliche Grundlage gibt. Die lokale Politik hat
offensichtlich keine anderen Probleme, so dass man sich
solche angstauslösenden Themen sucht, dann zum »Problem«
macht und die »Pseudolösung« als Erfolg verkauft.
Aschaffenburg kann keinen arsenfreien Schotter kaufen -
den gibt es nicht! |
|
Richelsdorfer Gebirge: Im Sommer 2017 wurden Bodenproben
in der Gemeinde Wildeck analysiert. Nun, auch hier
bedarf es keiner prophetischen Weitsicht, dass man
reichlich Schwermetalle, wie Arsen, nachweisen konnte.
Die geologischen Verhältnisse sind denen im Spessart um
Bieber sehr ähnlich; aber es gab dort wohl keine
Eisenerze und auch keine darauf fußende Eisenverhüttung.
Der Kupferschiefer in Richelsdorf wird von einer
hydrothermalen Co-Ni-Mineralisation durchschlagen ("Kobaltrücken").
Diese Vererzung ist der Fundort für sehr schöne
Skutterudit-Kristalle, die denen in Bieber sehr ähnlich
sehen; wenn es schöne Kristalle sind, stammen
die aus Richelsdorf. Und es gab dort eine Schmelz-Hütte
an einem Bach, in der die anstehenden Erze über einen
langen Zeitraum verarbeitet wurden. Die Folge der
Analysen sind gesperrte Flächen wie Spielplätze und eine
mediale Verunsicherung der Bevölkerung.
Das Ortsschild von Richelsdorf, aufgenommen am 30.04.2019 Kupferschiefer als Bestandteil einer Böschung bei Bauhaus, aufgenommen am 30.04.2019  Körniger Skutterudit als typisches Erz der Kobaltrücken um Richelsdorf aus der Mineraliensammlung von Dr. H. Gericke in Leipzig, Bildbreite 10 cm |
|
Nun sind die ausgestopften Tiere in den Schulen
Aschaffenburgs "entdeckt" worden: Die Tageszeitung Main-Echo
berichtet kurz vor Weihnachten 16.12.2017 auf der Seite
5 Report "Ausgestopfte Tiere mit Arsen: Gefahr für
Schüler? Lehrmaterial: Früheres Konservierungsmittel
krebserregend - Aschaffenburger Schulen haben reagert
und Bestände aufgelöst".
Ein Tierbalg oder ein Fell stellt für zahlreiche Insekten einen großen Nahrungsvorrat dar. Neben diversen Schmetterlingen (Motten) sind es die Speckkäfer, die solche Kunstwerke (Dermoplastiken) in kurzer Zeit zerstören können. Zur Verhinderung von Frasschäden wurden die Präparate bis vor wenigen Jahrzehnten mit einer Arsenik-Lösung (40 g Arsenik auf 0,1 l Wasser) bestrichen. Dabei verdunstet das Wasser und das Arsenik scheidet sich im Geweben als Feststoff aus und tötet beim Befall die fressenden Insekten. Wenn man etwas anderes verwendet, dann funktioniert das nur, wenn es Insekten tötet - und das tun ausschließlich Gifte, die im Laufe der Zeit nicht zerfallen und so ihre Giftigkeit behalten; da gibt es nicht so viele Substanzen. Gefährdet ist dabei eigentlich nur derjenige, der diese imprägnierten Gegenstände mit nassen Händen anfasst, so dass das Arsenik gelöst werden kann. Beim Anschauen besteht überhaupt keine Gefahr. |
| Bieber
(Biebergemünd): Wie in Richelsdorf, gab es Bieber
(mit Gassen, Röhrig, Rossbach und Webersfeld) einen
lange anhaltenden und intensiven Bergbau. Der fußt auf
einer geogenen Struktur, die es den Menschen
ermöglichte, Metalle wie Eisen, Mangan, Kupfer, Blei,
Silber und Kobalt in einem damals auskömmlichen Umfang
zu gewinnen. Gedanken um eine Schädigung der Umwelt und
auch sich selbst gab es so gut wie nicht, denn die
Weltordnung fußte auf einer von Gott gegebenen
Hierarchie, die als Schicksal hingenommen wurde. Der
letzte Bergbau wurde kurz nach der Weltwirtschaftskrise
eingestellt und seit dem nicht mehr aufgenommen. Was
blieb, sind die nicht abgebauten Bereiche der
metasomatischen Gesteine, die nicht bauwürdigen
Erzgänge, große Halden und sonstige Sachzeugen der
einstigen Tätigkeiten. In einer Hütte wurden die Erze
geschmolzen.
F. L. v. CANCRIN beschreibt 1787 die ersten Probleme mit den Schwermetallen in der Landwirtschaft. Dabei wurde in dem unterhalb gelegenen Kurmainz (aus Wirtheim und Kassel) eine Beeinträchtigung des Graswuches auf den Wiesen reklamiert (auf 20.00 fl.) und auch später entschädigt, wenn auch eine weit geringere Summe (CANCRIN 178:16ff). Es ist klar, dass diese Mischung aus geogener Anomalie und menschlichen Aktivitäten heute noch nachweisbar sind. So wurden die Bürger von Biebergemünd am 20.03.2018 informiert, dass die Grenzwerte für Arsen und Blei an einigen Stellen überschritten sind (siehe Gelnhäuser Neue Zeitung vom 22. März 2018 Seite 29 "Biebergemünd"). Gesperrter Spielplatz in Bieber, aufgenommen am 31.03.2018 Inzwischen wurde eine Zusammenfassung der Historie der Arsengeschichte von Bieber veröffentlicht (EMMRICH 2024) und als Altlast des Bieberer Bergbaus gedeutet. In dem kleinen werden die Ursachen der gegenwärtigen Maßnahmen aus historischen und aktuellen Unterlagen beschrieben. Die geologisch-mineralogischen Besonderheiten von Bieber finden keine Berücksichtigung. |
Der Schluss lautet:
Beim Wort oder Silbe Arsen: ruhig bleiben und erst
nachdenken.

Diverse Formen von Arsen und Gefäße mit Arsenverbindungen,
ausgestellt
im sehr sehenswerten Deutschen Apothekenmuseum im Schloss in
Heidelberg,
aufgenommen am 27.01.2013
Mineralbestimmung! Auf der Suche nach einem schönen Arsenolith mit großen Kristallen bekam ich folgenden Stück:  "Farblose Arsenolith-Kristalle (Arsenik) aus einer brennenden Kohlehalde des bis 1983 in Betrieb befindlichen und 1.005 m tiefen Pigeot-Schachtes in Crassier Saint-Pierre, La Ricamarie, Loire, Rhone-Alpes, Frankreich, wo die Wärme aus der brennenden Kohle den Arsenopyrit im Haldenkörper röstet. In den kälteren Teilen sublimiert das gasförmige Arsen zu Arsenolith und Claudetit. Bildbreite 2 cm" Mit diesen Informationen hatte ich das kleine Stück erhalten und es schien passend. So machte ich ein Foto und stellte es an passender Stelle auf diese Internetseite. Aber dann hatte ich wegen der Kristallform und des Glanzes Zweifel und untersuchte das Mineral. Das Beugungsmuster ließ sich sinnvoll keiner Phase zuordnen: 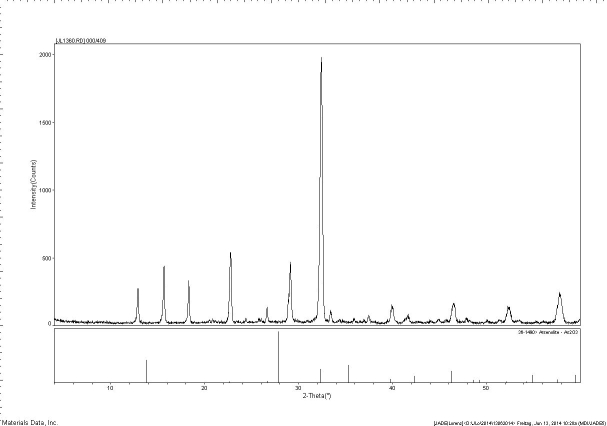 Das Beugungsmuster der Kristalle und darunter das Muster das Arsenolith, welches gar nicht passt. Eine passende Zuordung konnte noch nicht erfolgen. Der nächste Schritt war die Bestimmung der Elemente, die am Aufbau beteiligt sind. Das Ergebnis ist, dass da gar kein Arsen drin ist, sondern es besteht aus 2 Phasen: Einem Magnesium-Sulfat und einem Aluminium-Chlorid. Also muss man sehr vorsichtig sein, wenn man ungewöhnliche Mineralien anspricht oder kauft. In vielen Fällen ist nicht das drin was auf den Zetteln steht. Das gilt insbesondere auch für Arsenmineralien und die Folgen die davon abgeleitet werden. Wenn man sicher gehen will, kommt man um eine (oder mehrere) Analyse(n) nicht herum. Dass das Aufwand bedeutet und damit auch Geld kostet ist richtig, aber wenn davon Einschränkungen, finanzielle Auswirkungen oder andere weit reichende Folgen (z. B. Gesundheit) abhängen, dann führt kein anderer Weg zum Ziel. |


Gangstück aus hauptsächlich gediegen Arsen mit kleinen
Silbereinschlüssen, (im Bild wegen des metallischen Glanzes kaum
trennbar); an der Oberseite
schließt sich eine Gangbrekzie mit Calcit an, angeschliffen und
links frisch poliert,
Bildbreite 10 cm;
rechts nach 4 Wochen Lagerung in einem kühlen Raum "angelaufen",
so dass das graue ged. Arsen als Matrix gegen das noch silbrige
Silber erkennbar
wird,
Bildbreite 3 cm.
Im SDAG-Wismut-Bergwerk bei Pöhla im westlichen Erzgebirge stieß
man kurz vor der Schließung im Jahr 1990 auf der +120-m-Sohle in
einen Gang auf einen Silberanbruch aus Ged. Arsen mit reichlich
Gediegen Silber und Prousit (und ohne Uran) mit gediegen Arsen.
Der Gang war nach Augenzeugen bis zu 30 cm mächtig. Dabei wurden
einige Tonnen des Silbererzes gefördert. Die ungewöhnliche
Paragenese mit dem Arsen verhinderte zunächst eine Aufbereitung
und so wurde das Material aufgehaldet oder an Mineraliensammler
verkauft. Hätten mittelalterliche Bergleute einen solchen
Gang gefunden, wäre dies weithin bekannt geworden und der Ort wäre
wie Freiberg usw. gewachsen und "reich" geworden. Da das Gedigen
Silber im Roherz kaum sichtbar ist und die Stücke dunkelgau
anlaufen, hat man an den meisten Stücken das ged. Arsen zur
Wertsteigerung weggelöst (z. B. mittels H2O2),
um das metallische Silber frei zu legen. Das Silber liegt in der
Form von feinkristallinen Masse als filigrane Skelettkristalle
(hopper) vor und deutet auf ein schnelles Wachstum hin. Nach der
Bildung des Silbers wurden die verbliebenen Hohlräume mit Ged.
Arsen als hydrothermale Bildung ausgefüllt.

Glaskopfartiges, metallisches Arsen (Gediegen Arsen) als
"Scherbenkobalt"
mit einem Gewicht von 754 g aus dem Schacht 371 bei Schlema,
Bildbreite 13 cm

Graues, glaskopfartiges Gediegenes Arsen aus einem Erzgang mit
braunem
Siderit aus dem Gang H14F auf der 7. Sohle des Uranbergwerks #21
in
Pribram-Haje in Zentralböhmen der ehemaligen Tschechoslovakei,
gefunden 1983,
Bildbreite 5 cm
Literaturhinweise & Quellen:
ALLESCH, R. M. (1959): Arsenik. Seine Geschichte in Österreich.- Archiv für vaterländische Geschichte und Topographie 54. Band, 302 S., ohne Abb., [Verlag Fred. Kleinmayr] Klagenfurt.
ALLOWAY, B. J. (2013): Heavy Metals and Metalloids as Micronutrients for Plants and Animals.- p195 -209, 1 fig., tabs., in ALLOWAY, B. J. [ed.] (2013): Heavy Metals in Soils. Trace Metals and Metalloids in Soils and their Bioavilaility.- Environmental Pollution 22, 3rd ed., 613 p., figs., tabs., [Springer Science] Dordrecht.*
ANDERLE, H.-J., ROTHE, P. & SCHARPFF, H.-J. (2021): Taunus.- Sammlung Geologischer Führer Band 111, 305 S., 93 farb. Abb., 1 geologische Falt-Karte mit Aufschlusspunkten, [Gebrüder Borntraeger] Stuttgart.
Anonym (2003): (Mitteilungen der Länderarbeitsgemeinschaft Abfall (LAGA) 20 Anforderungen an die stoffliche Verwertung von Mineralischen Reststoffen/Abfällen - Technische Regeln - Stand: 6. November 2003. 127 S., ohne Ort und Verlag.
Anonym (2013): Die Medici. Geld, Macht & Mord.- National Geographic Heft März 2013, S. 40 - 69, über 20 farb. Abb., 1 Stammbaum, National Geographic Society - Gruner & Jahr, Hamburg.
Autorenkollektiv (2006): Arsenic.- Elements. An International Magazin of Mineralogy, Geochemistry, and Petrology Vol. 2, No. 2, p. 65 – 128, Mineralogical Society of America.
BANCROFT, P. & WELLER, S. (1993): Cornwall´s famous Mines.- The Mineralogical Record 24, Number 4 July/August 1993, p. 259 - 283, 28 figs., 2 tables, Tucson
BARI, H. (1983): Markirch/Elsass. Die Mineralien des berühmten Bergbaureviers.- Lapis Jahrgang 8, Heft Nr. 6 Juni 1983, S. 9 - 37, 66 Abb., als Fotos, Karten und Kristallzeichnungen, 2 Tab., [Christian Weise Verlag] München.
BIBRA, Freiherr E. von (1855): Die narkotischen Genußmittel und der Mensch.- 398 S., ohne Abb., [Wilhelm Schmid] Nürnberg.
BITZER, F. (2014): Zur Hydrologie im Übergangsbereich von Pfälzer Mulde, Mainzer Becken und Oberrheingraben (Exkursion I am 25. April 2014).- Jahresberichte und Mitteilungen des Oberheinischen Geologischen Vereins NF 96, S. 195 - 222, 15 Abb., 1 Tab., [Schweizerbart´sche Verlagsbuchhandlung] Stuttgart.
BLANKENBURG, H. J., GÖTZE, J. & SCHULZ; H. (1994): Quarzrohstoffe.- 2. Auflage, 296 S., mit 165 Abb., 80 Tab., [Deutscher Verlag für Grundstoffindustrie] Leipzig.
BOWELL, R. J., ALPERS, C. N., JAMIESON, H. E., NORDSTROM, K. D. & MAJZLAN, J. [eds.] (2014): Arsenic Environmental Geochemistry, Mineralogy, and Microbiology.- Reviews in Mineralogy & Geochemistry Volume 79, 635 p., zahlreiche SW- und wenige Farbabb., Diagramme, Tab., Mineralogical Society of America & Geochemical Society, Chantilly, Virginia, USA.
BURNS, PETER C. & FINCH, ROBERT [Eds.] (1999): Uranium Mineralogy, Geochemistry and the Environment.- Reviews in Mineralogy Vol. 38, 679 p., Mineralogical Society of America, Washington. DC.
CACARASSO & LINIAN (2013): The stomatological use of stones cited in the Kitab al-tasrif teratise (Abulcasis, 1000 CE).- in DUFFIN, C. J., MOODY, R. T. J. & GARDNER-THORPE, C. [eds.] (2013): A History of Geology and Medicine.- 490 p., Geological Society Special Publication 375, einige, teils farb. Abb., [Berfors Inforamtion Press Ldt.] Oxford.
CARLE, WALTER (1975): Die Mineral- und Thermalwässer von Mitteleuropa Geologie, Cheminismus, Genese.- 643 S., 14 Abb., 1.402 Analysen, 15 Karten in Mappe, [Wissenschaftliche Verlagsgesellschaft mbH] Stuttgart.
CHALINE, E. (2012): 50 Erdschätze die unsere Welt veränderten.- 224 S., zahlreiche farb. Abb., [Haupt Verlag] Bern.
DAIGLE, K. (2016): Gift im Trinkwasser.- Spektrum der Wissenschaft Heft April 2006, S. 70 - 79, 9 Abb., [Spektrum der Wissenschaft Verlagsgesellschaft mbH] Heidelberg.
DO SAMEIRO BARROSO (2013): Bezoar stones, magic, science and art.- in DUFFIN, C. J., MOODY, R. T. J. & GARDNER-THORPE, C. [eds.] (2013): A History of Geology and Medicine.- 490 p., Geological Society Special Publication 375, einige, teils farb. Abb., [Berfors Inforamtion Press Ldt.] Oxford.
EARL, B. (1996): The Cornish Arsenic Industry.- 32 p., 8 figs., [Penhellick Publications] Redruth, Cornwall.
EMMRICH, S. (2024): Arsen - eine Altlast des Bieberer Bergbaus.- S. 36 - 44, 1 Abb., 2 Tab.- in Autorenkollektiv (2024): Jahresheft des Geschichtsvereins Biebergemünd e. V.- 48 S., einige Abb., [ohne Verlag] ohne Ort.
EMSLEY, J. (2005): The Elements of Murder. A History of Poison.- 418 S., ohne Abb., [Oyford Unversity Press] Oxford UK
FALBE, JÜRGEN & REGNITZ, MANFRED [Hrsg.] (1989): Römpp Chemie Lexikon Band A – Cl.- 9. Aufl., S. 1 – 762, [Georg Thieme Verlag] Stuttgart.
FALBE, JÜRGEN & REGNITZ, MANFRED [Hrsg.] (1992): Römpp Chemie Lexikon Band T – Z.- 9. Aufl., S. 4.429 – 5.314, [Georg Thieme Verlag] Stuttgart.
FIEDLER, HANS-JOACHIM & RÖSLER, HANS JÜRGEN (1993): Spurenelemente in der Umwelt.- 2. Aufl., 385 S., [Gustav Fischer Verlag] Jena.
FITZ, S. (1984): Die Luminiszenz von Gläsern im UV-Licht. Eine Methoe zr Herkunftsbestimmung?.- S. 137 - 143, 1 Abb.- in GRIMM, C. [Hrsg.] (1984): Glück und Glas Zur Kulturgeschichte des Spessartglases.- Veröffentlichungen zur Bayerischen Geschichte und Kultur Nr. 2/84, 395 S., zahlreiche auch farb. Abb., [Verlag Kunst & Antiquitäten] München.
Gmelin-Institut für Anorganische Chemie und Grenzgebiete in der Max-Planck-Ges. z. Förderung der Wissenschaften [Hrsg.] (1971): Arsen.- Gmelins Handbuch der Anorganischen Chemie System-Nr. 17, 8. Aufl., 20 Figuren, [Springer Verlag] Berlin. (aktualisierter Nachdruck der Ausgabe von 1952).
GRANVILLE, D. (1838): LXV. Ueber arsenikhaltige Lichtkerzen. Aus einem im Namen einer Comission abgestatteten Berichte.- Journal für praktische Chemie 14. Band Jahrgang 1838 2. Band, S. 379 – 379, ohne Abb., Tab., Verlag von Johann Ambrosius Barth] Leipzig.
GRUBER, F. (2016): Vom Gold zum Radon-Heilstollen: Niedergang und Neuanfang des Edelmetallbergbaus in den Hohen Tauern zwischen dem 16. und dem 20. Jahrhundert.- Der Anschnitt. Zeitschrift für Kunst und Kultur im Bergbau 68. Jahrgang., Heft 1-2/2016, S. 14 - 34, 26 Abb., 4 Tab., Hrsg. von der Vereinigung der Freunde von Kunst und Kultur im Bergbau e. V., Deutsches Bergbau-Museum Bochum.
HAWKSLEY, L. (2018): Gefährlich schön. Giftige Tapeten im 19. Jahrhundert.- 256 S., zahlreiche Abb. im Text, 132 S. farbige Tapetennachdrucke als größere Seiten, [Gerstenberg Verlag] Hildesheim.
HELMUTH, J. H. (1808): Das Mineralreich.- Gemeinnützige Naturgeschichte der In- und Auslandes. Neunter und letzter Band, 2. Aufl., 506 S., ohne Abb., [Gehard Fleicher dem Jüngern] Leipzig.
HINTZE, C. (1904): Handbuch der Mineralogie Erster Band Elemente - Sulfide - Oxyde - Haloide - Crabonate - Sulfate - Borate - Phosphate Erste Abtheilung Elemente und Sulfide.- 1.208 S., mit 399 Abb. im Text, sehr zahlreiche Tabellen, [Verlag von Vit & Comp.] Leipzig.
HIRNER, A. V., REHAGE, H. & SULKOKSKI, M. (2000): Umwelt-geochemie Herkunft, Mobilität und Analyse von Schadstoffen in der Pedosphäre.- 836 S., 125 Abb., [Steinkopff Verlag] Darmstadt.
JÄGER, G. v. (1864): Ueber die Wirkungen des Arseniks auf Pflanzen im Zusammenhange mit Physiologie, Landwirtschaft und Medicinalpolizei.- 115 S., 4 Abb., [E. Schweizerbart´sche Verlagshandlung] Stuttgart.
JOACHIM, H. & DICK, R. (1994): Rollenbergminerale. Eine mineralogische Studie der gangförmigen und schichtgebundenen Vererzungen am Rheingrabenrand nördlich von Bruchsal.- 68 S., Katalog zur Sonderausstellung „Mineralien des Rollenbergs“, 104 Farbbilder, 10 SW-Fotos und 5 Zeichnungen, 11 unpag. Seiten Inserate [Eigenverlag] Pforzheim.
KAHL, A. (2013): Viel Neues. Neues aus dem AGS.- Der Sicherheitsingenieur 6/2013, S 15 - 17, ohne Abb., Tab.,
KARSTEN, C. J. B. (1831): System der Metallurgie geschichtlich, statistisch, theoretisch und technisch Vierter Band.- 629 S., ohne Abb., Tab., [G. Reimer] Berlin.
Kernforschungszentrum Karlsruhe [Hrsg.] (1991): Radioaktivität Risiko – Sicherheit.- 2. Aufl., 80 S.,
KIRNBAUER, T. (2007): Rezente und fossile Mineral- und Thermalwasseraustritte am Taunusrand (Exkursion D am 12. April 2007).- Jber. Mitt., oberrhein. geol. Ver., N. F. 89, S. 167- 192, 14 Abb., Stuttgart.
KIRNBAUER, T. (2008): Hydrothermale Bildungen des Thermalwassersystems von Bad Nauheim (Wetterau) und dessen Alter.- Jber. Wetterau. Ges. ges. Naturkunde 158. Jg., 2. Bd., S. 39 – 96, 8 Abb., 11 Tab., Hanau.
KLEINE, S., LEES, B. K. & SOUTHWOOD, M. (2014): Oripiment from Twin Creeks mine, Nevada, USA.- Minerals. The Collector´s Newspaper 2014 Issue #8, 24 S., [Spiriferminerals.com].
KOPP, J. H. (1807): Ueber den zu Bieber im Hanauischen einbrechenden Kobaltvitriol und das ihn begleitende Arsenikoxyd.- Taschenbuch für die gesammte Mineralogie, mit Hinsicht auf die neuensten Entdeckungen, Erster Jahrgang, S. 104 - 119, [J. Chr. Hermann] Frankfurt am Main.
KRAEMER [Hrsg.] (1906): Der Mensch und die Mineralien.- Dritter Abschnitt von Der Mensch und die Erde; 420 S., sehr viele Abb. im Text und teils farb., gefaltete Tafeln im Text, [Deutsches Verlagshaus Bong & Co] Berlin.
LENZ, H. O. (1856): Gemeinnützige Naturgeschichte Fünfter Band: Mineralreich.- 3. verbesserte Aufl., 444 S., mit dreizehn Tafeln im Anhang; [Becker`sche Buchhandlung] Gotha.
LIU, J., HUANG, X., WANG, W., ZHANG, W. & DONG, F. (2014): Experimental and model studies on comparison of As (III and V) removal from synthetic acid mine drainage by bone char.- Mineralogical Magazine February 2014 Vol. 78(1), pp. 73 - 89, 5 tab., 9 fig., Mineralogical Society.
LEONHARD, K. C. v. (1846): Taschenbuch für die Freunde der Geologie in allgemein faßlicher Weise bearbeitet.- Zweiter Jahrgang, 248 S., 3 Stahlstiche, mehrere Abb. im Text, [E. Schweizerbart´sche Verlagsbuchhandlung] Stuttgart.
LORENZ, J. mit Beiträgen von Okrusch, M., Geyer, G., Jung, J., Himmelsbach, G. & Dietl, C. (2010): Spessartsteine. Spessartin, Spessartit und Buntsandstein - eine umfassende Geologie und Mineralogie des Spessarts. Geographische, geologische, petrographische, mineralogische und bergbaukundliche Einsichten in ein deutsches Mittelgebirge. VI + 912 S., 2.532 meist farbigen Abb., 134 Tab. und 38 Karten (davon 1 auf einer ausklappbaren Doppelseite), [Helga Lorenz Verlag] Karlstein.
MARKL, G. (2017): Schwarzwald Lagerstätten und Mineralien aus vier Jahrhunderten Band 4 – Südlicher Schwarzwald.- 880 S., sehr viele Farbabb., Edition Krüger-Stiftung, [Bode Verlag] Lauenstein.
MARQUARDT, H. & SCHÄFER, S. [Hrsg.] (2004): Lehrbuch der Toxikologie.- 2. Aufl., 1.348 S., 456 Abb., 342 Tab., [Wissenschaftliche Verlagsgesellschaft mbH] Stuttgart.
MARTRAUD, A. (2013): Les Mineraux de Sainte-Marie-aux-Mines.- 208 S., sehr viele farb. Abb., Les Editions du Piat.
MERIAN, ERNEST [Hrsg.] (1991): Metals and Their Compounds in the Environment Occurence, Analysis and Biological Relevance.- 1.438 p., tab., [VCH Verlagsgesellschaft mbH] Weinheim
MOORE, CARLETON B. & MASON, BRIAN (1985): Grundzüge der Geochemie.- 340 S., 97 Abb., 66 Tab., [F. Encke Verlag] Stuttgart].
QUIRING, H. (1946): Arsen.- Die metallischen Rohstoffe ihre Lagerungsverhältnisse und ihre wirtschaftliche Bedeutung 8. Heft, 168 S., 16 Abb., [Ferdinand Encke Verlag] Stuttgart.
PARASCANDOLA, J. (2012): King of Poisons. A History of Arsenic.-196 p., some b&w pictures, [Potomac books] Washington DC.
PEKOV, I. V., ZUBKOVA, N. V., YAPASKURT, V. O., BELAKOVSKY, D. I., LYKOVA, I. S., VIGASINA, M. F., SIDOROV, E. G. & PUSHCHAROVSKY, D. YU. (2014): New arsenate minerals from tte Arsenatnaya fumarole, Tolbachik volcano, Kamchatka, Russia. I. Yuramarinite Na7(Fe3+, Mg, Cu)4(AsO4)6.- Mineralogical Magazine Journal of Mineral Science Vol. 78 (4), August 2014, p. 905 - 917, 8 figs., 5 tab., The Mineralogical Society, Bath.
PUFFER, J. H. (1980): Toxic Minerals.- The Mineralogical Record 11, Number 1 January/February 1980, p. 5 - 11, 2 figs., 1 table, Tucson
RAVENSCROFT, P., BRAMMER, H. & RICHARDS, K. (2009): Arsenic Pollution. A global synthesis.- 588 p., 106 figs., 113 tab., [Wiley-Blackwell] Chichester GB.
RENTZ, O & MARTEL C. (1998): Analyse der Schwermetallströme in Steinkohlefeuerungen - Einfluß der Kohlesorten und des Lastzustandes-.- 254 S., zahlreiche Tab. und Diagramme, Deutsch-Französisches Institut für Umweltforschung (DFIU) Universität Karlsruhe.
RICKARD, D., MUSSMANN, M. & STEADMAN, J. A. (2017): Sedimentary Sulfides.- in Elements Vol. 13 Number 2 April 2017, p. 117 - 122, 5 figs., 1 tab.,
ROSENBERG, F. & RÖHLING, H.-G. [Hrsg.] (1999): Arsen in der Geosphäre.- Schriftenreihe der Deutschen Geologischen Gesellschaft, Heft 6: 127 - 130, 4. Abb., 1 Tab., Hannover.
RÖSLER, HANS JÜRGEN & LANGE, HORST (1976): Geochemische Tabellen.- 2. Aufl., 674 S., [F. Encke Verlag] Stuttgart.
RÖSSLERN, B. (1700): Speculum Metallurgiae Politissimum. Oder Hell polierter Berg-Bau-Spiegel/ Darinnen zu befinden: Wie man Bergwerk suchen/ausschürffen/mit Nutzen bauen/allenthalben wohl anstellen/ ...- 200 S., mit zahlreichen Holzschnitten, Tab., [Johann Jacob Wincklern] Dresden, Nachdruck der Edition „libri rari“, Th. Schäfer GmbH, Hannover.
ROTH, H. J. (2013): Unser täglich Gift. Tatsächliche und vermeintliche Schadstoffe im Alltag.- 255 S., ohne Abb., Tab., [S. Hirzel Verlag] Stuttgart.
RÜDE, T. R. (1996): Beiträge zur Geochemie des Arsens.- Karlsruher Geochemische Hefte 10, 206 S., 56 Abb., Schriftenreihe des Instituts für Petrographie und Geochemie, Eigendruck der Universität Karlsruhe.
SIEGEL, F. R. (2002): Environmental Geochemitry of Potentally Toxic Metals.- 218 p., 40 fig., 33 tab., [Springer Verlag] Berlin.
SINDERN, S., GÖRTZ, A. & GRONEN, L. (2016): Historische und rezente anthropogene Schwermetalleinträge im Bereich des Montanwirtschaftsstandorts Stolberg (Rheinland) (Exkursion B am 29. März 2016).- Jahresberichte und Mitteilungen des Oberrheinischen Geologischen Vereins Neue Folge Band 98, S. 15 - 31, 4 Abb., [E. Schweizerbart´sche Verlagsbuchhandlung] Stuttgart.
STENGEL-RUTKOWSKI, W. (2009): Hydrogeologischer Führer zu den Kochsalz-Thermen von Wiesbaden.- 26 S., 7 Abb., Nassauischer Verein für Naturkunde, Wiesbaden.
SUCHER, "SU" A. (2011): Hittrach. Arsenik Humane & Equine Arznei und Leistungssteigerung.- 136 S., ohne Abb. [novum publishing GmbH] ohne Ort.
TRUEB, L. F. (1996): Die chemischen Elemente. Ein Streifzug durch das Perisodensystem.- 416 S., 132 Abb. davon 28 in Farbe, [S. Hirzel Verlag] Stuttgart.
VIALARON, C. (1995): L´Arsenic. sond historie, son usage, son exploitation dans departement de la Haute-Loire. 128 S., einige Bilder, teis in Farbe, Grubenrisse, Karten, [Impiminere Deloche] Lamastre, Ardeche.
VÖLKEL, J. (2003): Bodenbelastung durch Schwermetalle.- S. 112 -113, 3 Abb. in Institut für Länderkunde [Hrsg.] (2003): Nationalatlas Bundesrepublik Deutschland Band 2. Relief, Boden und Wasser.- 174 S., zahlreiche Karten, Pläne, Grafiken, Skizzen, Abb., [Spektrum Akademischer Verlag] Heidelberg
VOLKE, K. (2009): Chemie im Altertum unter besonderer Berücksichtigung Mesopotamiens und der Mittelmeerländer.- 690 S., einige Abb. und Tab., [Akademische Buchhandlung] Freiberg.
VOLKMER, MARTIN (1990): Die natürliche Strahlenbelastung.- 9. Aufl., 64 S., Hamburgische Electricitäts-Werke AG.
WALTHER, Dr. (1842): Sicherste Methode die Anwesenheit des Arseniks bei Arsenikvergiftungen zu ermitteln, im Auftrag der k. Akademie der Medicin in Paris bekannt gemacht von Buffon, Abelon, Pelletier, Chavalier und Caventon.- 44 S., ohne Abb., [J. J. Lenter´schen Buchhandlung] München.
WEINER, K. L. & HOCHLEITNER, R. (1983): Steckbrief Gediegen Arsen.- Lapis Jahrgang 8, Heft Nr. 6 Juni 1983, S. 6 - 7, 1 Abb., [Christian Weise Verlag] München.
WENEZL, W. W. (2013): Arsenic.- p. 241 - 282, 2 figs., 2 tab., in ALLOWAY, B. J. [ed.] (2013): Heavy Metals in Soils. Trace Metals and Metalloids in Soils and their Bioavilaility.- Environmental Pollution 22, 3rd ed., 613 p., figs., tabs., [Springer Science] Dordrecht.
WIBERG, N. (1995): Holleman-Wiberg. Lehrbuch der Anorganischen Chemie.- 101. Aufl., 2.033 S., zahlreiche Strukturen, Tab., [Walter de Gruyter] Berlin.
WIESER, O. (1903): Über den sogenannten natürlichen Arsenik.- 31 S., Inaugural-Dissertation verfasst und der Hohen medizinischen Fakultät der Königl. Bayer. Julius-Maximilians-Universität Würzburg zur Erlangung der Doktorwürde, ohne Abb., [Memminger´s Buchdruckerei & Verlagsanstalt] Würzburg.
WHORTON, J. C. (2010): The Arsenic Centrury. How Victorian Britain was Poisened at Home, Work, and Play.- 412 p, wenige Abb., [Oxford University Press] Oxford UK.
*Das Buch ist ohne jede Farbe gedruckt, hat eine Klebebindung und wird für einen Preis von 181,85 € verkauft! Der unverhältnismäßig hohe Preis ist der Grund für die geringe Verbreitung, was zu einer noch geringeren Auflage führt - und dies wieder zu einem noch höheren Preis. So ist abzusehen, dass solche Werke nur noch elektronisch angeboten werden.
Dass Auripigment kein seltenes Mineral ist, zeigt
diese Schachtel mit derbem
Auripigment aus einem nicht näher bezeichneten Vorkommen in
China, welches zu
einem Preis von 30 € das Kilogramm auf der Mineralienbörse von
St.-Marie-aux-Mines
angeboten wurde,
aufgenommen am 23.06.2016
Arsenmineralien und Bücher aus Frankreich. Man hat
hier weniger Berührungsängste
als in Deutschland: Sonderausstellung auf der Mineralien- und
Fossilien-börse in
St.-Marie-aux-Mines, Vogesen,
aufgenommen am 28.06.2019
In der Sonderschau der Minerlienbörse in München
2021 wurde neben einem durchbohrten
Franklinit (ZnFe23+O4)
Zwillinge des seltenen Minerals Cahnit (Ca2B(AsO4)(OH)4,
rechts auf dem Kubus) ausgestellt.
